Informazioni generali
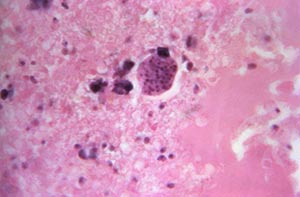 La toxoplasmosi è una zoonosi causata dal Toxoplasma gondii, un
microrganismo che compie il suo ciclo vitale, estremamente complesso e
diverso a seconda dell’ospite, solo all'interno delle cellule. Il parassita
può infettare moltissimi animali (dai mammiferi agli uccelli, dai rettili ai
molluschi) e può trasmettersi da un animale all’altro attraverso
l’alimentazione con carne infetta. Il Toxoplasma condii non si trova
solo nella carne, ma anche nelle feci di gatto e nel terreno in cui abbia
defecato un gatto o un altro animale infetto.
La toxoplasmosi è una zoonosi causata dal Toxoplasma gondii, un
microrganismo che compie il suo ciclo vitale, estremamente complesso e
diverso a seconda dell’ospite, solo all'interno delle cellule. Il parassita
può infettare moltissimi animali (dai mammiferi agli uccelli, dai rettili ai
molluschi) e può trasmettersi da un animale all’altro attraverso
l’alimentazione con carne infetta. Il Toxoplasma condii non si trova
solo nella carne, ma anche nelle feci di gatto e nel terreno in cui abbia
defecato un gatto o un altro animale infetto.
Sintomi, prevenzione e trattamento
Nell’infezione da Toxoplasma gondii è possibile distinguere due fasi
successive: la prima (toxoplasmosi primaria) è caratterizzata da un periodo
di settimane o mesi in cui il parassita si può ritrovare nel sangue e nei
linfonodi in forma direttamente infettante. È la fase sintomatica della
toxoplasmosi, che si accompagna a ingrossamento delle linfoghiandole,
stanchezza, mal di testa, mal di gola, senso di "ossa rotte", a volte febbre
e ingrossamento di fegato e milza. Esistono poi casi di toxoplasmosi
primaria complicati da sintomi gravi, quali l'infiammazione della zona
visiva dell’occhio (corioretinite, che può compromettere la vista) e
dell’encefalo, oltre a sintomi attribuibili a una malattia autoimmune.
Quest'ultima eventualità è frequente nei malati di Aids o nei soggetti
trapiantati, per i quali spesso l’evoluzione è drammatica, perché la
risposta alla terapia è insufficiente.
Il soggetto che contrae una toxoplasmosi resta protetto
per tutto l’arco della vita da recidive, perché risponde all’infezione con
produzione di anticorpi e linfociti specifici.
La risposta del soggetto al Toxoplasma gondii
determina il passaggio alla seconda fase della toxoplasmosi (toxoplasmosi
postprimaria), caratterizzata dall’assenza di segni clinici e di laboratorio
dell’infezione acuta, ma con la persistenza del parassita nell’organismo, "incistato"
nei muscoli e nel cervello. Se le difese immunitarie vengono meno (sia per
malattia, sia per trattamenti medici), il microrganismo può tornare
aggressivo, riprodursi e indurre nuovi danni.
La toxoplasmosi è ad alto rischio nel caso in cui venga
contratta in gravidanza: l'infezione può infatti passare al bambino
attraverso la placenta, provocando in determinate circostanze malformazioni
o addirittura l'aborto o la morte in utero. La toxoplasmosi rappresenta
dunque un importante elemento di cui tenere conto nell'ambito della
salute materno-infantile.
Allo stato attuale non esiste un vaccino contro la
toxoplasmosi: non è quindi possibile garantirne la prevenzione assoluta. Ci
sono però una serie di comportamenti e di pratiche che possono ridurre
notevolmente il rischio di contrarre questa malattia.
Uno studio che ha coinvolto diversi centri in Europa, tra i quali anche due centri italiani (uno a Napoli e uno a Milano), pubblicato sul British Medical Journal nel 2000, indica tra le principali fonti di infezione nelle donne gravide il consumo di carne poco cotta. Dai risultati emerge infatti che i fattori di rischio principali sono legati all’alimentazione (dal 30 al 63% dei casi dovuti all’assunzione di carne poco cotta). È quindi necessario evitare di assaggiare la carne mentre la si prepara e lavarsi molto bene le mani sotto acqua corrente dopo averla toccata. Lo stesso studio evidenzia che un’altra importante fonte di contaminazione è rappresentata dalla manipolazione della terra degli orti e dei giardini, dove animali infetti possono aver defecato. È quindi necessario che, chi svolge attività di giardinaggio, si lavi molto bene le mani prima di toccarsi la bocca o la mucosa degli occhi. Lo stesso vale per il consumo di ortaggi e frutta fresca, che dev’essere lavata accuratamente sotto acqua corrente.
Infine, negli ultimi anni si è ridimensionata
l’attenzione nei confronti del gatto come portatore della malattia, in
particolare se si tratta di un gatto domestico, alimentato con prodotti in
scatola e la cui lettiera è cambiata tutti i giorni (le cisti del parassita
si schiudono dopo tre giorni a temperatura ambiente e alta umidità). Il vero
serbatoio della toxoplasmosi è invece rappresentato dai gatti randagi, che
si infettano cacciando uccelli e topi contaminati, e che possono defecare
nel terreno rilasciando Toxoplasma anche per diverse settimane.
Nel caso in cui la donna dovesse essere contagiata
durante la gravidanza, è possibile bloccare la trasmissione dell'infezione
al bambino attraverso un trattamento antibiotico mirato. Il trattamento più
utilizzato è quello con spiramicina, un antibiotico ben tollerato sia dalla
madre sia dal feto. Una revisione dei lavori scientifici pubblicati (consultabile sul BMJ, 1999)
sulle prove di efficacia della terapia in gravidanza della toxoplasmosi
evidenzia la difficoltà di produrre una stima dell’efficacia del trattamento
per la scarsità di studi randomizzati confrontabili. Inoltre uno
studio multicentrico (consultabile su Am. J. Obstet. Gynecol., 1999) ha
dimostrato che esistono combinazioni antibiotiche più efficaci (pirimetamina
e sulfadiazina) almeno nell’impedire la comparsa di postumi all’anno di
vita: l’uso di questa combinazione è d’obbligo quando la trasmissione
dell’infezione al feto sia dimostrata attraverso l’amniocentesi. Nel caso in
cui il trattamento non sia stato adeguato o sia iniziato troppo tardi, il
bambino potrebbe avere una malattia grave già visibile alla nascita.
Con le attuali possibilità di trattamento, almeno il
90% dei bambini con toxoplasmosi congenita nasce senza sintomi evidenti e
risulta negativo alle visite pediatriche di routine. Solo attraverso
indagini strumentali più raffinate possono essere rilevabili piccole
anomalie a carico dell’occhio e dell’encefalo.
Le probabilità di trasmissione dell’infezione materna
al feto aumentano man mano che la gravidanza progredisce: i bambini la cui
mamma abbia contratto la toxoplasmosi dopo le 16-24 settimane
di gestazione appaiono spesso normali alla nascita, anche se opportune
indagini strumentali possono mettere in rilievo alcune anomalie. I feti
contagiati nelle prime settimane di gravidanza, invece, sono quelli che
subiscono le conseguenze più gravi dell’infezione congenita: interruzione
spontanea della gravidanza, idrocefalia, lesioni cerebrali che possono
provocare ritardo mentale ed epilessia, ridotta capacità visiva che può
portare fino alla cecità.
Diagnosi
Poiché la malattia è spesso asintomatica, idealmente
sarebbe bene conoscere il proprio stato prima della gravidanza, e cioè
sapere se nel proprio siero siano presenti gli anticorpi per la toxoplasmosi.
Si tratta di un semplice esame del sangue: chiamato Toxo-test, permette di
classificare le donne in tre classi: "protetta", "suscettibile" o "a
rischio".
L’infezione induce nel corpo la produzione di
immunoglobuline specifiche: nella prima fase della malattia (quella
pericolosa per il nascituro) vengono prodotte IgM, successivamente (in una
fase meno rischiosa) gli anticorpi prodotti sono di classe IgG. Il Toxo-test
permette quindi di verificare l’assenza o la presenza di anticorpi, e, in
questo secondo caso, di evidenziare se si è ancora in una fase a rischio o
se invece la donna è da considerarsi protetta. Se la condizione della donna
non è nota prima della gravidanza, allora il Toxo-test deve essere
prontamente eseguito durante la gravidanza, con la prima serie di esami del
sangue entro le prime otto settimane di gestazione. Se la donna è protetta
(ha gli IgG) il test non deve più essere ripetuto. Nel caso in cui invece la
gestante sia "suscettibile", e quindi non abbia gli IgG né gli IgM, deve
eseguire almeno altri due controlli nel corso della gravidanza, a 20 e 36
settimane, per escludere la possibilità di essersi infettata e che quindi il
bambino rischi di contrarre una toxoplasmosi congenita.
Nel caso in cui il test dia come risultato la presenza
di anticorpi IgM, l’infezione in gravidanza è comunque solo sospetta. Si
procede quindi con test sierologici più sofisticati presso centri di
riferimento di riconosciuta esperienza sia per accertare la diagnosi sia,
eventualmente, per disegnare una terapia. Se l’infezione è confermata, il
nascituro, anche se apparentemente sano, dovrà essere seguito per almeno
tutto il primo anno di vita da un centro specializzato per poter escludere
eventuali danni cerebrali e visivi che insorgano nei mesi successivi.
