Il contributo delle ostetriche al Sistema di farmacovigilanza e alla segnalazione di sospette reazioni avverse a farmaci nel Lazio
Elena Tammelleo¹, Angela Giusti¹, Bruno Caffari² e Sofia Colaceci³
¹Ostetrica, libera professionista; ²Centro Nazionale di Epidemiologia, Sorveglianza e Promozione della Salute, Istituto Superiore di Sanità, Roma; ³Dipartimento di Biomedicina e Prevenzione, Università degli Studi di Roma Tor Vergata
SUMMARY (Midwives’ contribution to pharmacovigilance system and adverse drug reactions reporting in Latium Region: a survey on knowledge, attitudes and practices) - This study describes knowledge, attitudes and practices on adverse drug reactions (ADR) reporting and the pharmacovigilance (PV) system, using a questionnaire administered to 188 midwives. Only 23% of sample knew the PV system and 6% reported ADR throughout their careers. Nevertheless, midwives didn’t report to PV system, but their reports seem to be just mere communications to the physician. This survey shows that PV is still difficult to access for nonmedical healthcare professionals and it represents an educational need.
Key words: pharmacovigilance; adverse drug reaction reporting systems; midwifery
Introduzione
Il principale impulso alla nascita della farmacovigilanza (FV) è legato al disastro della talidomide, un farmaco commercializzato negli anni Cinquanta e Sessanta e impiegato nel trattamento dei disturbi del primo trimestre di gravidanza come antiemetico e ipnotico. Le donne trattate con talidomide diedero alla luce neonati con gravi alterazioni congenite dello sviluppo degli arti. Da questo disastro scaturì la necessità di sorvegliare in modo sistematico i farmaci, non solo prima dell’immissione in commercio (fase pre marketing), ma anche e soprattutto dopo (fase post marketing), per individuare la comparsa di reazioni avverse; in seguito a tale evento alcuni Stati europei attivarono e/o implementarono le strutture di farmacovigilanza (1).
Un rilevante campo di interesse nell’ambito della FV è rappresentato dai farmaci usati in gravidanza, per i rischi di teratogenicità, e durante l'allattamento per i rischi legati alla possibile assunzione del farmaco da parte della madre e del lattante. Questo è legato da un lato all’esclusione di questi gruppi di popolazione dalle sperimentazioni pre marketing, dall’altro alla carenza di studi epidemiologici post marketing.
Va inoltre sottolineato che le donne consumano mediamente più farmaci degli uomini (2), ma sono meno rappresentate negli studi pre marketing. Per tale motivo, oltre che per le ciclicità ormonali mensili e i cambiamenti legati alle diverse fasi della vita, le donne sono soggette a una maggiore incidenza e gravità delle reazioni avverse da farmaci (adverse drug reactions - ADR) (3).
L’ostetrica accompagna la donna in tutte le fasi della vita e si trova pertanto nelle migliori condizioni per assicurare un attento monitoraggio delle possibili ADR.
Questo studio ha l’obiettivo di descrivere le conoscenze, gli atteggiamenti e le pratiche delle ostetriche sulla FV e sulla segnalazione di sospette ADR.
Materiali e metodi
L’indagine è stata svolta nei dipartimenti materno-infantili di 4 ospedali di Roma, includendo tutte le ostetriche in servizio. Le strutture sono state selezionate su criteri di convenienza per l’alto numero di dipendenti eleggibili. L’indagine è stata condotta adattando un questionario strutturato, anonimo e autocompilato, precedentemente utilizzato nell’ambito delle attività della Commissione Regionale di Farmacovigilanza, rivolto ai medici di medicina generale (4).
Il questionario è suddiviso in 4 sezioni: conoscenze, atteggiamenti, pratiche e dati socioanagrafici. Per indagare le conoscenze, è stata utilizzata una prova oggettiva di 13 quesiti con 3 opzioni di risposta, di cui una sola corretta.
Per la valutazione della prova oggettiva di conoscenza è stato utilizzato il software SITA (Sistema per l’ITem Analysis), prendendo in considerazione i punteggi percentuali individuali e medi di risposte corrette. I dati sono stati sottoposti ad analisi statistica descrittiva, con l’ausilio del software Epi-Info v. 3.5. Per valutare se vi fosse associazione tra l’atteggiamento “la segnalazione è compito esclusivo del medico” (espresso su scala Likert da “completamente in disaccordo” a “completamente d’accordo”) e l’aver segnalato almeno 3 casi di ADR nella propria carriera, è stato utilizzato il test esatto di Fisher. La pratica di segnalazione è stata definita come "abituale" se le segnalazioni di sospette ADR erano ≥ a 3, "occasionali" se <3.
Risultati
Tra marzo e novembre 2011 sono stati somministrati 188 questionari, con un tasso di rispondenza dell’85% (159/188). Il 95% degli intervistati era costituito da donne e il 5% da uomini con età media, rispettivamente, di 40 e 42 anni. L’anzianità media di servizio era di 17 anni (range 0-38).
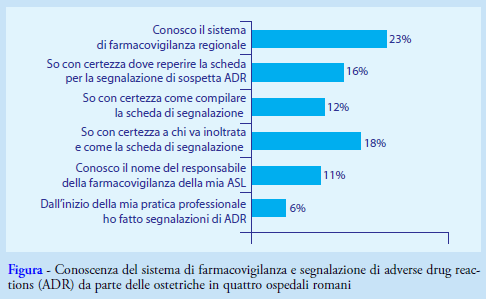
Rispetto alla conoscenza delle procedure di segnalazione delle ADR, il 23% dichiara di conoscere il sistema di FV, il 16% sa dove reperire la scheda, il 12% sa come compilarla, il 18% sa a chi inoltrarla. Solo l’11% conosce però il nome del responsabile della FV della propria struttura a cui indirizzare la scheda, e solo il 6% dichiara di aver inoltrato segnalazioni di ADR (Figura).
Esiste grande eterogeneità del livello complessivo di informazione sul sistema di FV tra le diverse strutture, con una variabilità che va da un massimo di 58,6% a un minimo di 5,7%. Tutte le segnalazioni effettuate da ostetriche provengono dalla struttura con il maggior livello di informazione.
Per quanto riguarda gli atteggiamenti positivi, il 58% dichiara di avere tempo per segnalare, il 74% ritiene che i dati siano utili e l’82% esprime la convinzione che le proprie segnalazioni apportino un contributo importante al sistema di FV. La procedura di segnalazione è giudicata eccessivamente burocratica dal 44%, il 19% ritiene che sia compito esclusivo del medico e il 9% pensa che potrebbe essere utilizzata ai fini di un procedimento legale contro il segnalatore. La percentuale di risposte esatte alla prova oggettiva di conoscenza è risultata del 61%.
Le ostetriche che dichiarano di aver segnalato almeno 3 ADR nella propria carriera (n=9) ritengono con maggior frequenza (77,8% rispetto al 36,3% di coloro che hanno effettuato meno di 3 segnalazioni, p<0,02) che si tratti di un proprio compito e non di una mansione esclusiva del medico.
Infine, il 90% dichiara di essere interessato a eventi formativi sulla FV.
Discussione e conclusioni
Nonostante un atteggiamento favorevole nei confronti della segnalazione delle ADR, emergono una scarsa conoscenza generale del sistema di FV da parte delle ostetriche e un'altrettanta scarsa consapevolezza del proprio ruolo. Pur sapendo che la segnalazione rientra tra i propri compiti, le ostetriche che hanno dichiarato di aver segnalato non hanno di fatto seguito la procedura che prevede l’invio della scheda al responsabile della FV. Da un approfondimento eseguito attraverso la Rete Nazionale di Farmacovigilanza, si evince che le ostetriche non risultano tra le categorie di segnalatori. In concreto, sembra più plausibile che le ostetriche che hanno dichiarato di aver segnalato almeno un caso intendano, in realtà, una segnalazione al medico, svolgendo così un mero ruolo di “sentinella”. Questo dato è confermato da un analogo studio che ha coinvolto gli infermieri ospedalieri (5).
Dall’indagine emerge, inoltre, che solo una ridotta parte del campione conosce il nome del responsabile della FV della propria struttura. Secondo la letteratura, il ruolo del responsabile della FV è determinante: laddove il personale conosce il suo nominativo, l’informazione complessiva sul sistema di FV è significativamente più alta (6). Sembra, inoltre, che nella formazione di base questo argomento non venga affrontato in modo sufficiente, e probabilmente per tale motivo le ostetriche hanno espresso un elevato interesse in merito. A tal proposito, gli interventi di comunicazione e di formazione sul sistema di FV sembrano essere efficaci nel determinare un miglioramento degli atteggiamenti e un aumento delle segnalazioni (7). La normativa europea in materia di FV è stata di recente modificata, con l’adozione nel 2012 del Regolamento UE 1235/2010 e della Direttiva 2010/84/UE. Gli obiettivi della nuova normativa rendono ancora più urgente una partecipazione attiva dei professionisti sanitari, oltre che dei cittadini, al sistema di segnalazione delle ADR. Le ostetriche possono avere un ruolo chiave nel sistema di segnalazione e nel promuovere la partecipazione attiva e diretta delle donne. Per tale motivo, la FV dovrebbe rientrare nella formazione curriculare ed essere oggetto di specifici eventi nell’ambito dell’educazione continua in medicina.
Dichiarazione sui conflitti di interesse
Gli autori dichiarano che non esiste alcun potenziale conflitto di interesse o alcuna relazione di natura finanziaria o personale con persone o con organizzazioni, che possano influenzare in modo inappropriato lo svolgimento e i risultati di questo lavoro.
Riferimenti bibliografici
1. AIFA. Panorami e percorsi. Una nuova vita per la talidomide. BIF 2009;16(3):113-6.
2. Gruppo di lavoro OsMed. L’uso dei farmaci in Italia. Rapporto nazionale anno 2011. Roma: Il Pensiero Scientifico Editore; 2012.
3. Franconi F, Montilla S, Vella S. Farmacologia di genere. Torino: SEED; 2010.
4. Giusti A. I percorsi di formazione per la Farmacovigilanza: costruzione e valutazione. Relazione presentata al Congresso della Commissione regionale per le attività di Farmacovigilanza della Regione Lazio. Roma, 31 gennaio 2011.
5. De Angelis A, Giusti A, Caffari B, et al. Farmacovigilanza in ambito infermieristico: uno studio quali-quantitativo. XXI Seminario Nazionale di Farmacoepidemiologia. La valutazione dell’uso e della sicurezza dei farmaci: esperienze in Italia. Atti. Roma, 10 dicembre 2012. Roma: Istituto Superiore di Sanità; 2012 (ISTISAN Congressi 12/C6).
6. Heideiro MT, Figueiras A, Polinia J, et al. Influence of pharmacists’attitudes on adverse drug reaction reporting: a case-control study in Portogal. Drug Safety 2006;29(4):331-40.
7. Caffari B, Giusti A, Nati G, et al. I percorsi della formazione per la Farmacovigilanza nella Regione Lazio: costruzione e valutazione. XII Conferenza Nazionale di Sanità Pubblica, Società Italiana di Igiene (SItI). Atti. Roma, 11-15 ottobre 2011:683.

 Bollettino epidemiologico nazionale
Bollettino epidemiologico nazionale