L’impatto dei virus influenzali in Italia nella stagione 2020-21 durante la pandemia di COVID-19
Donato Grecoa, Caterina Rizzob, Simona Puzellic, Anna Caragliad, Francesco Maraglinod, Antonino Bellac
b Area Funzionale Percorsi clinici ed Epidemiologia, Direzione Sanitaria, Ospedale Bambino Gesù, Roma
c Dipartimento di Malattie Infettive, Istituto Superiore di Sanità, Roma
d Direzione Generale della Prevenzione Sanitaria, Ministero della Salute, Roma
Citare come segue: Greco D, Rizzo C, Puzelli S, Caraglia A, Maraglino F, Bella A. L’impatto dei virus influenzali in Italia nella stagione 2020-21 durante la pandemia di COVID-19. Boll Epidemiol Naz 2021; 2(2):1-6. DOI: https://doi.org/10.53225/BEN_013
Impact of 2020-21 seasonal influenza in Italy during the COVID-19 pandemic
Introduction
Influenza and COVID-19 are high transmission pathologies which have a different median incubation period. Although the symptoms are similar, people are more likely to be affected by severe and/or critical COVID-19 infection than severe and/or critical influenza infection. It is well proven that school closure and personal protection measures (mask-wearing and social distancing) are effective in reducing the spread of infection. This study aims to highlight the impact of 2020-21 seasonal influenza on the Italian population during the COVID-19 pandemic and to identify possible reasons for that.
Materials and methods
To describe the impact of influenza on the population, data from the Integrated Influence Surveillance InfluNet and vaccination coverage in Italy in the 2020-21 season were used. Influenza Like Illness (ILI) incidence rates per thousand patients and influenza vaccination coverage (%) were calculated on the total population and by age group.
Results
In Italy, the 2020-21 flu season was characterized by a low incidence of ILI and the absence of circulation of flu viruses. Compared to the previous season, influenza vaccination coverage increased by almost 7% in the total population (23.7% vs 16.8%, 2020-21 and 2019-20 season respectively) and almost 11% in the elderly (65.3% vs 54.6%, 2020-21 and 2019-20 season respectively).
Conclusions
For the first time in the last twenty-one years, since InfluNet surveillance was established, there has not been a seasonal flu epidemic. Although seasonal influenza vaccination coverage has increased compared to previous seasons, especially among children, it cannot be the only reason for the disappearance of the seasonal flu epidemic. Certainly several factors contributed: the increase in vaccination coverage, an immune memory effect and, probably, a viral competition in which the new coronavirus prevailed. Still, all this is not enough to justify the total disappearance of influenza. Based on these considerations, we think that the disappearance of seasonal influenza is mainly due to the stringent protection measures implemented to counter the spread of COVID-19: mask-wearing, distancing, hand washing, school and business closures have been very effective in eliminating the seasonal flu epidemic.
Key words: influenza; influenza vaccination coverage; nonpharmaceutical measures
Introduzione
Nell’autunno 2020 destava preoccupazione, tra gli addetti ai lavori, la co-circolazione del SARS-CoV-2 e dei virus influenzali. Per tale ragione, il Ministero della Salute ha indicato di anticipare, per quanto possibile, la campagna vaccinale antinfluenzale e di aumentare le coperture vaccinali nella popolazione, ciò non solo per non sovraccaricare il Servizio Sanitario Nazionale, ma anche per effettuare più facilmente una diagnosi differenziale, dato che i due patogeni si presentano con una sintomatologia molto simile.
L’influenza e il COVID-19 sono due patologie che hanno, infatti, in comune alcuni aspetti, anche se altri li distinguono nettamente. Entrambi provocano infezioni con un’alta trasmissibilità: il numero riproduttivo (R0), cioè il numero di infezioni secondarie generate da un individuo infetto, del virus SARS-CoV-2 è compreso tra 2 e 2,5, superiore a quello dell'influenza (1).
Il periodo di incubazione mediano (il tempo dall'infezione alla comparsa dei sintomi) è più breve per l’influenza: 3 giorni contro i 5-6 giorni del SARS-CoV-2 (1).
I bambini sono i maggiori responsabili della trasmissione dei virus influenzali nella comunità, mentre per il COVID-19 la fascia d’età 0-19 anni è meno colpita di quella degli adulti, con tassi di attacco più bassi.
Se la sintomatologia per i due virus è simile, la quota della popolazione colpita da infezione grave e/o critica nel COVID-19 è superiore a quella osservata per l'infezione influenzale. I soggetti più a rischio di una grave infezione influenzale sono i bambini, le donne in gravidanza, gli anziani, i soggetti con patologie croniche preesistenti e gli immunodepressi. Per il COVID-19, l'età avanzata e le condizioni sottostanti aumentano il rischio di infezioni gravi. La mortalità per COVID-19 sembra superiore a quella per l'influenza, in particolare l'influenza stagionale (1).
Influenza e COVID-19 si trasmettono per via aerea: l’individuo infetto emette con il suo respiro, ancor più con tosse e starnuti, goccioline di vapore acqueo contenente materiali cellulari e virus in grandi quantità (droplet). L’individuo esposto, a sua volta, inala queste particelle umide permettendo l’impianto del virus sulle mucose delle prime vie aeree. Il soggetto, se non è entrato mai in contatto con COVID-19 o influenza, viene aggredito da queste particelle che si moltiplicano velocemente, con una preferenza per l’albero respiratorio, tranne nel caso in cui l’organismo ha una forte risposta immunitaria dovuta ad anticorpi prodotti da una precedente infezione o dal vaccino.
È possibile, per quanto rara, la trasmissione da mani o superfici contaminate con cellule viventi contenenti il virus, anche se resta prevalente la trasmissione respiratoria e i fattori di rischio a essa associati, quali affollamento, scarsità di ricambi ambientali d’aria, spazi chiusi, ma anche fattori individuali come il fumo di sigaretta che rende le mucose delle vie respiratorie più permeabili ai virus e le malattie dell’apparato respiratorio, quali bronchite cronica e asma.
Per quanto riguarda l’influenza, sono principalmente i bambini che trasmettono l’influenza, poiché sono privi di memoria immunologica storica verso i virus influenzali.
È ben dimostrato che la chiusura delle scuole primarie e anche l’adozione di misure di protezione individuale (mascherine e distanziamento) sono efficaci nel ridurre la trasmissione dell’infezione (2, 3).
Questo studio si propone l’obiettivo di evidenziare l’impatto dei virus influenzali nella popolazione italiana durante la stagione 2020-21 nel contesto della pandemia di COVID-19.
Materiali e metodi
La sorveglianza integrata dell’influenza in Italia, InfluNet, si basa su due reti: un sistema di medici sentinella in cui oltre 1.000 medici di medicina generale e pediatri di libera scelta segnalano all’Istituto Superiore di Sanità, ogni settimana, le sindromi simil-influenzali (influenza like illness, ILI) osservate tra i propri assistiti e una rete di sorveglianza virologica composta da 22 laboratori di riferimento regionale per l’influenza che analizzano i campioni clinici inviati dai medici sentinella e segnalano settimanalmente l’eventuale positività ai virus influenzali su centinaia di campioni biologici (4-6).
Per valutare l’impatto delle ILI sulla popolazione italiana è stata calcolata l’incidenza (per 1.000 assistiti) totale e per fascia di età. Per stabilire il livello dall’incidenza raggiunta nella stagione 2020-21, rispetto alle stagioni passate, sono state utilizzate le soglie calcolate con il metodo MEM (moving epidemic method) dell’European Centre for Disease Prevention and Control - ECDC (7, 8). Per la stagione 2020- 21 sono state stimate le seguenti soglie: 3,16 casi per 1.000 assistiti (livello basale), 9,37 (intensità bassa), 14,37 (intensità media), 17,36 (intensità alta), oltre 17,36 (intensità molto alta). La copertura vaccinale (%) della popolazione italiana totale e per fascia di età (6-23 mesi, 2-4 anni, 5-8 anni, 9-14 anni, 15-17 anni, 18-44 anni, 45-64 anni e >64 anni) è stata calcolata rapportando il numero di dosi somministrate dalle Regioni sulla popolazione italiana residente al 1° gennaio 2021 (9).
Risultati
I risultati della sorveglianza InfluNet nella stagione 2020-21
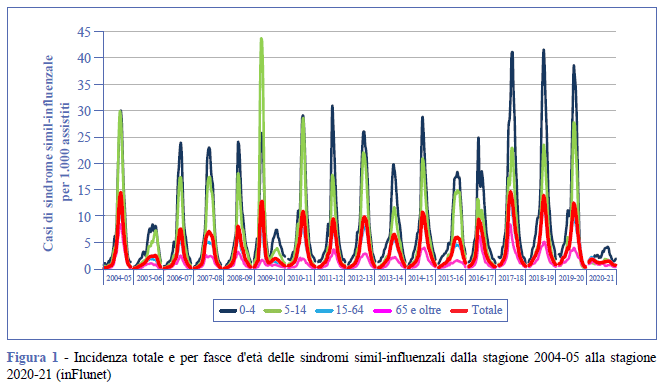
Le sindromi simil-influenzali stagionali hanno una loro regolarità: il numero di casi inizia a crescere alla fine di ogni anno, raggiunge il picco stagionale alla fine del mese di gennaio dell’anno successivo e dura fino a marzo. Nella Figura 1 è riportato il trend stagionale nazionale dell’incidenza delle ILI, totale e per fascia di età, dalla stagione 2004-05 a quella 2020-21. Si osservano stag ioni con bassa incidenza e stagioni in cui i virus influenzali sono stati più aggressivi, con picchi di incidenza totale che hanno superato i 14 casi per 1.000 assistiti, come evidenziato nelle stagioni 2017-18, 2018-19.
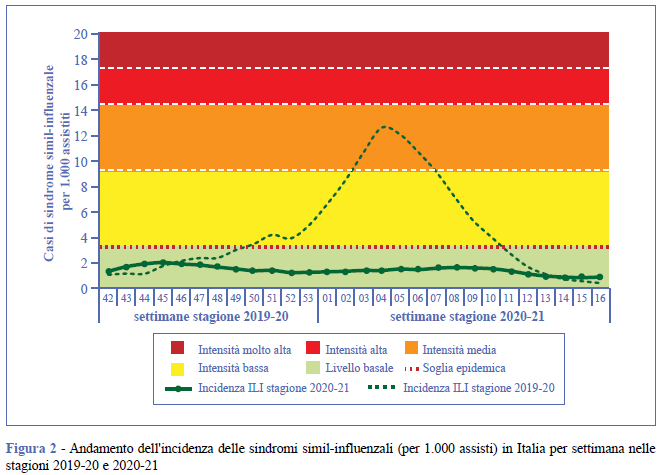
La stagione 2020-21 è stata caratterizzata da una bassa incidenza di ILI che è rimasta sotto il valore soglia di 3,16 casi per 1.000 assistiti per l’intera stagione. Questo risultato dimostra che il periodo epidemico delle ILI non è mai iniziato, dal momento che per definizione tale periodo inizia quando la curva supera la soglia basale (per la stagione 2020-21, 3,16 casi per 1.000 assistiti) e termina quando torna a livelli al di sotto di tale soglia (Figura 2).
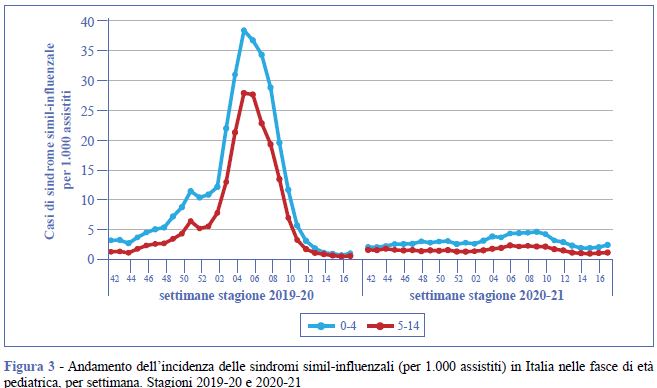
A fine gennaio 2021 l’incidenza delle ILI era pari a 1,4 casi per 1.000 assistiti, mentre nella stagione precedente (2019-20), nello stesso periodo, era di 12,6 casi per 1.000 assistiti. Il numero di casi di ILI si è mantenuto molto basso anche nelle fasce di età pediatrica, età in cui si osserva generalmente l’incidenza più elevata (Figura 3).
Dal punto di vista virologico, su un totale di oltre 6.800 campioni clinici analizzati dai laboratori della rete InfluNet dall’inizio della sorveglianza, nessun virus influenzale è stato isolato per tutta la durata della sorveglianza (dalla 46a settimana del 2020 alla 16a settimana 2021) su tutto il territorio nazionale (6).
Un dato in netta controtendenza con i milioni di casi che l’influenza stagionale provoca ogni anno. Le possibili spiegazioni dell’assenza di circolazione dei virus influenzali nel contesto della pandemia da COVID-19 posso dipendere: dalla copertura vaccinale antinfluenzale raggiunta nella popolazione, dalla memoria immunitaria e dalla competizione virale.
La copertura vaccinale antinfluenzale in Italia nella stagione 2020-21
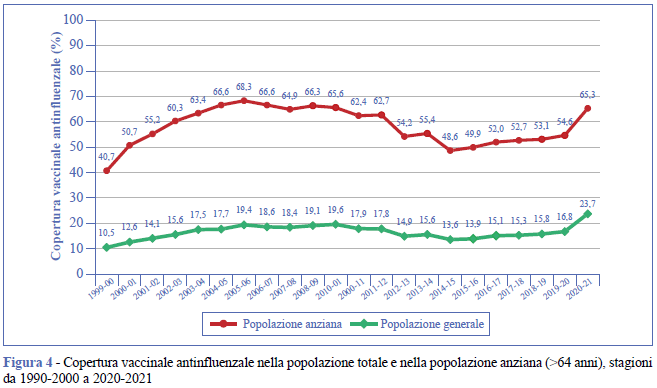
Nell’autunno 2020 si è vaccinato il 23,7% degli italiani, quasi sette punti percentuale in più rispetto all’anno precedente (16,8%) (Figura 4). Sono state somministrate poco più di 14 milioni di dosi di vaccini antinfluenzali, una quantità ben superiore agli anni precedenti, grazie all’intensa campagna informativa condotta. La copertura negli anziani (>64 anni) ha raggiunto il 65,3%, quasi 11 punti percentuali in più rispetto al precedente anno in cui era pari al 54,6% (Figura 4).
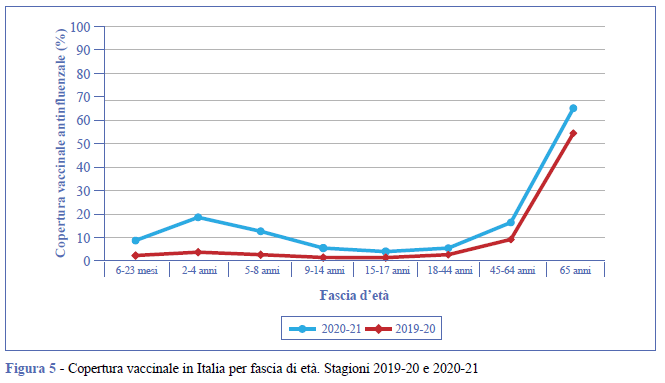
L’aumento della copertura vaccinale, comunque, rispetto allo scorso anno, è generalizzato in tutte le fasce di età, ma soprattutto in quelle pediatriche, in cui è stata sempre molto bassa e presente solo in alcune Regioni. La copertura vaccinale antinfluenzale sotto i due anni di età è passata dal 2,8%, rilevata nella stagione 2019-20, al 9,2% nella stagione 2020-21. Il maggiore incremento si osserva nella fascia di età 2-4 anni, in cui si è passati dal 4,2% al 19,0% nell’ultima stagione; nella fascia 5-8 anni l’incremento è stato più contenuto, passando dal 3,1% della stagione 2019-20 al 13,1% nella stagione 2020-21 (Figura 5).
La memoria immunitaria
Sebbene i virus influenzali non diano una memoria immunitaria a vita, come avviene per altri virus patogeni - ed è per questo che è necessario vaccinarsi ogni anno - una qualche immunità antinfluenzale resta nell’organismo; non è sufficiente per proteggere da una nuova infezione influenzale, ma probabilmente ne attenua l’impatto sia in termini di incidenza che di severità (10). Tale osservazione si basa sull’evidenza che l’epidemia stagionale di influenza colpisce molto di più i bambini rispetto ad adulti e anziani, non solo per la loro maggiore vita di comunità nelle scuole, ma soprattutto per la loro scarsa esperienza di epidemie influenzali; i bambini, quindi, hanno poca o nulla memoria immunitaria.
Lo spostamento di nicchia ecologica
L’ecologia di molti virus può portarli a competere tra loro. Infatti, se una popolazione è vaccinata contro alcuni sottotipi di un virus, nuovi sottotipi dello stesso virus prendono il sopravvento. Anche l’influenza stagionale ogni anno si affaccia su una popolazione ove viaggiano molti altri virus a trasmissione respiratoria che provocano malattie simil-influenzali, ma è nel pieno del picco epidemico influenzale che si osserva come i virus influenzali emergono e come la loro frequenza diventa predominante. Nello scorso inverno ha circolato in modo molto diffuso il virus SARS-CoV-2 che potrebbe aver contribuito all’eliminazione del virus influenzale stagionale (11), anche se non può spiegarne l’eliminazione completa.
Discussione e conclusioni
La stagione influenzale è stata caratterizzata da una bassa incidenza di ILI e dall’assenza di circolazione dei virus influenzali. Tutti i 6.818 campioni clinici analizzati dalla rete dei laboratori di InfluNet sono risultati negativi ai virus influenzali. Di questi, il 20% (1.470 su 6.818) sono risultati positivi al virus SARSCoV- 2. Per la prima volta negli ultimi ventuno anni, da quando cioè è stata istituita la sorveglianza InfluNet, non c’è stata un’epidemia stagionale di influenza, malattia che, come è noto, colpisce mediamente 5-6 milioni di italiani ogni anno e causa la morte di quasi diecimila persone ogni stagione (12). Questo fenomeno ha caratterizzato non solo il nostro Paese ma molti Paesi del mondo, primo tra tutti l’Australia. L’influenza non è, comunque, completamente sparita in Europa: l’ECDC riporta che dall’inizio della stagione 2020-21, su un totale di 682.485 campioni raccolti, 791 sono risultati positivi all’influenza; di questi, 396 (50,1%) appartenevano ai virus di tipo A e 395 (49,9%) al tipo B (6).
Ma allora quali sono i motivi che hanno portato alla scomparsa del virus influenzale nella stagione 2020-21 in Italia? Nonostante le coperture vaccinali abbiano avuto un incremento rispetto alle scorse stagioni, passando, nella popolazione generale dal 16,8% del precedente anno al 23,7% e dal 54,6% al 65,3% nella popolazione anziana (>64 anni) e considerando il forte incremento di tali coperture nelle fasce di età pediatriche, la sola copertura vaccinale non può giustificare la scomparsa dell’epidemia influenzale stagionale in Italia. Anche il residuo di memoria immunitaria acquisito dalla popolazione nel corso degli anni può spiegare solo in parte la limitata incidenza dell’influenza stagionale (mediamente 5-6 milioni di casi di ILI ogni inverno su una popolazione di circa sessanta milioni di persone (l’8-10%). Anche la competizione virale che ha visto il prevalere del nuovo coronavirus sui virus simil-influenzali può aver avuto il suo peso, ma tutti questi fattori non possono giustificare la totale scomparsa dell’influenza.
In Italia hanno fortemente contribuito ad annullare la circolazione dei virus influenzali le stringenti misure di protezione individuale messe in campo per contrastare il COVID-19: mascherine, distanziamento sociale, frequente lavaggio delle mani, chiusura di scuole ed esercizi commerciali.
Una riflessione definitiva sull’efficacia preventiva di queste misure, che hanno avuto un costo importante per la popolazione anche in termini economici e di salute mentale, potrà avvenire solo con evidenze solide. Oggi si può parlare di prevenzione da COVID-19 solo relativamente alla vaccinazione di massa, mentre la comunità scientifica è concorde nel classificare le misure di contenimento come strumenti utili alla mitigazione del danno (13).
Una pandemia causata da un nuovo virus, i cui effetti e la cui evoluzione è difficile da prevedere, ha comportato la necessita di adottare misure che non hanno avuto precedenti nella storia contemporanea. Sulla base di questa esperienza la comunità scientifica dovrà costruire una solida e permanente cultura della preparedness, vero strumento di prevenzione e controllo dei rischi pandemici.
Conflitti di interesse dichiarati: nessuno
Finanziamenti: nessuno.
Authorship: tutti gli autori hanno contribuito in modo signifi cativo alla realizzazione di questo studio nella forma sottomessa.
Riferimenti bibliografici
-
World Health Organization: Coronavirus disease (COVID-19): Similarities and differences with influenza. 17 March 2020; ultimo accesso 15/7/2021.
-
Nafisah SB. Alamery AH, Al Nafesa A, Aleid B, Brazanji NA. School closure during novel influenza: a systematic review. J Infect Public Health, 2018;11(5), 657-661. doi: 10.1016/j. jiph.2018.01.003
-
Aledort JE, Lurie N, Wasserman J, Bozzette SA. Nonpharmaceutical public health interventions for pandemic influenza: an evaluation of the evidence base. BMC Public Health 2007 Aug 15;7(1):1-9. doi 10.1186/1471-2458-7-208
-
Protocollo Operativo InfluNet & CovidNet: Stagione 2020-21; ultimo accesso 15/7/2021.
-
Rapporto InfluNet epidemiologico. N. 23 del 1 maggio 2021. Stagione Influenzale 2020–2021; ultimo accesso 15/7/2021.
-
Rapporto InfluNet virologico. N. 24 del 28 aprile 2021. Stagione Influenzale 2020-2021; ultimo accesso 15/7/2021.
-
Vega T, Lozano JE, Meerhoff T, Snacken R, Mott J, Ortiz de Lejarazu R, et al. Influenza surveillance in Europe: establishing epidemic thresholds by the Moving Epidemic Method. Influenza Other Respir Viruses 2013;7:546-58. doi: 10.1111/j.1750- 2659.2012.00422.x
-
Vega T, Lozano JE, Meerhoff T, Snacken R, Beauté J, Jorgensen P,, et al. Influenza surveillance in Europe: comparing intensity levels calculated using the Moving Epidemic Method. Influenza Other Respir Viruses. 2015 Sep;9(5):234-46. doi: 10.1111/ irv.12330.
-
Istat. https://demo.istat.it; ultimo accesso 15/7/2021.
-
Dugan HL, Guthmiller JJ, Arevalo P, Huang M, Chen YQ, Neu KE, et al. Preexisting immunity shapes distinct antibody landscapes after influenza virus infection and vaccination in humans. Sci Transl Med. 2020 Dec 9;12(573):eabd3601. doi: 10.1126/scitranslmed.abd3601
-
Schroeder D, Van Etten, JL, Jones IM, Paweska JT, Shi Z, Abdel-Moneim AS. (Ed). Host And Pathogen Mechanisms Underpinning Viral Ecology And Emerging Infections. Frontiers Media SA; 2021.
-
Rizzo C, Bella A, Viboud C, Simonsen L, Miller MA, Rota MC, S et al. Trends for influenza-related deaths during pandemic and epidemic seasons, Italy, 1969-2001. Emerg Infect Dis. 2007;13(5):694- 699. doi:10.3201/eid1305.061309
-
Qualls N, Levit A, Kanade N, Wright- Jegede N, Dopson S, Biggerstaff M, et al. Community Mitigation Guidelines to Prevent Pandemic Influenza - United States, 2017. Recommendations and Reports April 21 2017; 66(1):1–34. https://www.cdc.gov/...

 Bollettino epidemiologico nazionale
Bollettino epidemiologico nazionale