Implementazione di un sistema di screening per indirizzare la popolazione potenzialmente a rischio di reazioni avverse da vaccino COVID-19 in un hub di secondo livello: Lombardia, 12 maggio 2021-12 maggio 2022
Paolo Marraccinia, Matteo Letzgusb, Navpreet Tiwanab, Marco Dubinia, Alessandra Piattib, Francesco Masic, Flaminia Gentiloni Silverib
a Struttura Semplice Allergologia, Fondazione IRCCS Cà Granda Ospedale Maggiore Policlinico, Milano
b Direzione Medica di Presidio, Fondazione IRCCS Cà Granda Ospedale Maggiore Policlinico, Milano
c Scuola di Specializzazione in Medicina del Lavoro, Università degli Studi di Milano
Citare come segue: Marraccini P, Letzgus M, Tiwana N, Dubini M, Piatti A, Masi F, Gentiloni Silveri F. Implementazione di un sistema di screening per indirizzare la popolazione potenzialmente a rischio di reazioni avverse da vaccino COVID-19 in un hub di secondo livello: Lombardia, 12 maggio 2021-12 maggio 2022. Boll Epidemiol Naz 2023;4(1):18-24. DOI: https://doi.org/10.53225/BEN_061
A second level vaccination center in Lombardy (Italy) during the COVID-19 emergency (May 12th 2021-May 12th 2022) in order to support and monitor the allergic reactions
Introduction
Allergic reactions due to vaccines for coronavirus disease 2019 were observed since the beginning of the vaccination campaign all over the world.
Materials and methods
An oriented check list, based on the guidelines of the Italian allergy societies, was used by the first level vaccination center, to select subjects eligible for a second level of vaccination in protected hospital facility with allergist support. Moreover, patients with allergic reactions at the first dose were evaluated at the second level center where selected cases executed either allergy skin tests for COVID-19 vaccine additives or in vitro Basophil Activation Tests.
Results
During the period May 12th 2021 - May 12th 2022, the second level vaccination center carried out a sum of 17,380 vaccinations in a campaign of 1,850,399 doses administered. There was a significant statistical difference between Vaxzevria and mRNA vaccines in terms of reactions after first administration (p <0.001). No reactions were observed in Jcovden vaccine and only one case with Nuvaxovid. At the second dose only 30 subjects underwent cutaneous tests and 50 subjects BAT. No relevant positive allergic tests emerged in the 80 selected subjects. 15 subjects practiced off-label fractional vaccination. We didn’t observe anaphylaxis or allergic reactions due to the second and third dose.
Discussion and conclusions
The adoption of a check list was useful to select patients to refer to the second level center and proceed to mass vaccination in low-risk patients. The reactions that occurred at the first dose were presumably related to the nocebo effect. The allergy approach should be extremely circumscribed in perspective and well-organized, avoiding resorting to excessive evaluations or diagnostics.
Key words: SARS-COV-2; anaphylaxis; vaccines
Introduzione
La vaccinazione di massa per il COVID-19 ha comportato un notevole impegno da parte delle strutture sanitarie per la valutazione complessiva dei pazienti da sottoporre a vaccinazione, tra cui, di un certo rilievo, quella allergologica. La Food and Drug Administration e i Centers for Disease Control and Prevention di Atlanta hanno stimato reazioni anafilattiche con un tasso pari a 2,5% su 11,1 milioni di dosi di vaccini con mRNA (1, 2). È ormai noto che gli adiuvanti, preservanti e stabilizzanti di varie tipologie di vaccino, senza escludere l’agente infettivo del vaccino stesso, che può agire come trigger della reazione allergica, sono causa di tali reazioni (3).
In Italia, dopo l’avvio della vaccinazione nel dicembre del 2020, le reazioni avverse ai vaccini sono state segnalate dall’Agenzia Italiana del Farmaco (4) e una lista degli eccipienti è stata oggetto di analisi da parte della comunità scientifica, focalizzando l’interesse sul polietilenglicole (PEG) per entrambi i vaccini a mRNA, Comirnaty e Spikevax, sul trometamolo per il Spikevax, e sul polisorbato 80 (può presentare una possibile cross-reattività con PEG) per i vaccini ad adenovirus (Vaxzevria) (5).
Il 15 gennaio 2021 sono state pubblicate le linee di indirizzo per la gestione dei pazienti a rischio di reazioni allergiche ai vaccini anti COVID-19 della Società Italiana di Allergologia, Asma e Immunologia Clinica (SIAAIC) e dell’Associazione degli Allergologi Immunologi Italiani Territoriali e Ospedalieri (AAIITO) (6). Le linee di indirizzo hanno rappresentato uno strumento per definire il rischio allergologico di soggetti con pregresse reazioni allergiche, come anafilassi severa (coinvolgimento del sistema cardiovascolare e/o respiratorio) da qualsiasi causa o da causa non nota, asma non controllato, diagnosi di mastocitosi, reazioni allergiche a precedenti vaccini o a PEG e polisorbati (Figura 1). I pazienti con almeno una delle suddette condizioni avrebbero dovuto essere preventivamente inviati a visita allergologica con un accesso preferenziale e programmabile alla visita specialistica, al fine di effettuare una diagnostica specifica che permettesse di stratificare il rischio. In questa strategia, le linee di indirizzo ponevano diversi vincoli sulla vaccinazione dei soggetti allergici. Veniva suggerita una approfondita analisi delle pregresse reazioni a farmaci, e in particolare degli additivi PEG e polisorbati, con un ampio elenco di possibili farmaci implicati. La platea dei candidati a una valutazione allergologica risultava quindi estesa e di difficile gestione, vista la situazione dei Servizi di allergologia, depotenziati a causa dell'emergenza pandemica.
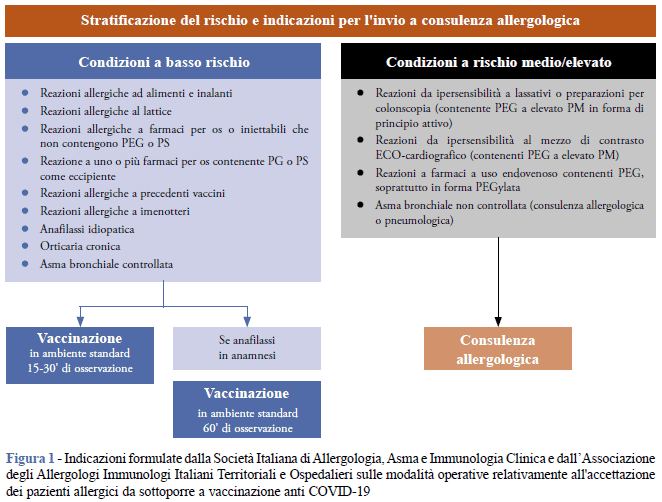
Tenendo conto della necessità di una risposta immediata, anche in considerazione del notevole numero di vaccinazioni da praticare, l’utilizzo di uno strumento di rapida esecuzione e lettura (scheda anamnestica) è stato ritenuto fondamentale. Pertanto, approntare un centro vaccinale satellite di secondo livello (Padiglione Ponti Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico Milano) per i casi valutati come critici negli hub di primo livello (Palazzo Scintille e Padiglione Fiera a Milano, centri massivi in Regione Lombardia), o per chi aveva presentato reazioni alla prima somministrazione, ha avuto lo scopo di supportare le prestazioni nell’hub vaccinale di primo livello.
Obiettivo del presente lavoro è quello di descrivere l’organizzazione di un centro vaccinale di secondo livello e di stimare le reazioni avverse, in particolare quelle allergiche, in una popolazione selezionata.
Materiali e metodi
Sulla base di un’attenta disamina della letteratura scientifica, delle condizioni cliniche potenzialmente a rischio e delle indicazioni riportate nelle linee di indirizzo è stata realizzata una scheda anamnestica, somministrata dal medico vaccinatore, opportunamente informato e formato, in fase di accettazione del paziente (Tabella 1).

Tale scheda ha permesso di discriminare i soggetti da vaccinare in hub di primo livello con osservazione prolungata senza necessità di invio al secondo livello, mentre sono stati vaccinati in ambiente ospedaliero protetto (Padiglione Ponti) i casi di reazione alla prima dose (Tabella 2). Pertanto nell’hub vaccinale di primo livello, i pazienti valutati come potenzialmente a maggior rischio di reazioni avverse che necessitavano di un approfondimento con lo specialista allergologo, sono stati inviati al centro di secondo livello tramite prenotazione interna con indicazione di luogo, data e ora dell’appuntamento. Presso il centro di secondo livello, strutturato con postazioni di medici vaccinatori affiancati dall’allergologo in consulenza e supporto, è stata riesaminata la scheda anamnestica compilata nell’hub di primo livello, e deciso il percorso più idoneo, indicando o l’immediata esecuzione della vaccinazione in assenza di elementi ostativi (la vaccinazione avveniva in area protetta con osservazione di almeno un’ora, assistenza infermieristica del reparto di Anestesia e Rianimazione, monitoraggio dei parametri vitali dei pazienti valutati più critici e pronta disponibilità all’intervento dei medici del suddetto reparto, dislocati in un’area contigua; nel caso di osservazioni prolungate vi era la possibilità di trasferimento in pronto occorso, presente nello stesso complesso), o l’esecuzione di approfondimenti clinici: test cutanei allergologici per gli eccipienti dei vaccini anti COVID-19, in base alle linee di indirizzo della SIAAIC e dell’AAIITO (6). I test in vitro, test di attivazione dei basofili (BAT) per i vari eccipienti PEG, polisorbato e trometamina (7) sono stati prescritti ai pazienti che non accettavano l’esecuzione dei test in vivo.
L’analisi statistica condotta è di tipo descrittivo, con il numero di somministrazioni effettuate e valori percentuali nei cicli vaccinali eseguiti. Il test del χ2 è stato eseguito per valutare il ricorso a vaccinazione protetta in seguito a reazioni insorte alla prima somministrazione per tipologia di vaccini. Per l’analisi statistica è stato utilizzato il software Stata 14 (Stata Corp 2015).

Risultati
La popolazione che ha avuto accesso ai centri vaccinali di primo e di secondo livello ha superato il mezzo milione (Figura 2) nel periodo compreso tra il 12 maggio 2021 e il 12 maggio 2022. Le vaccinazioni effettuate per la prima dose nell’hub di secondo livello sono state 3.482, pari allo 0,67% dei soggetti vaccinati. Nessuno dei pazienti che ha effettuato la prima dose nel centro protetto di secondo livello ha presentato reazioni di natura allergica.
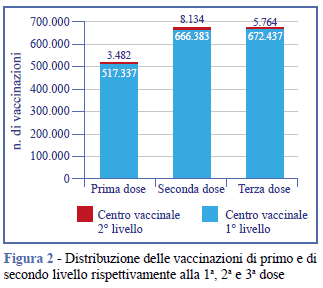
Per la seconda dose si osserva un incremento di 4.652 (0,90%) di accesso al secondo livello, a causa del manifestarsi di reazioni di sospetta natura allergica (sintomi cutanei e/o respiratori insorti entro le 6 ore dalla somministrazione) alla prima dose nel centro vaccinale di primo livello. Il numero delle vaccinazioni eseguite per le tre dosi nei centri vaccinali primari e nel centro di secondo livello viene riportato nella Tabella 3.

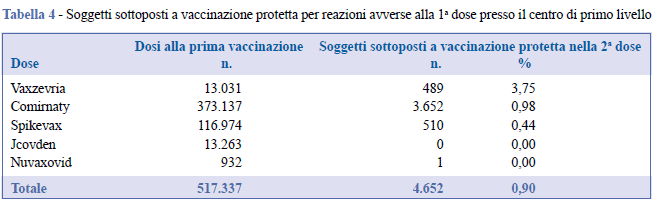
In merito ai soggetti sottoposti a vaccinazione protetta alla seconda dose, 489 hanno ricevuto Vaxzevria, 3.652 Comirnaty e 510 Spikevax, pari rispettivamente al 3,75%, 0,98% e 0,44% delle somministrazioni effettuate al centro vaccinale di primo livello alla prima dose per tipo di vaccino (Tabella 4). Si osserva una differenza statisticamente significativa tra Vaxzevria e i vaccini a mRNA in termini di invio a vaccinazione protetta in seguito a reazioni insorte alla prima somministrazione (p < 0,001). Non ci sono stati accessi per Jcovden al secondo livello e un solo caso di Nuvaxovid è pervenuto al secondo livello, non presentando criticità alla seconda somministrazione.
Dei 4.652 valutati ex novo alla seconda dose, 80 soggetti, pari all’1,7%, hanno effettuato approfondimenti allergologici in base all’anamnesi, alla documentazione clinica e al trattamento farmacologico effettuato dopo la prima somministrazione. Trenta soggetti sono stati sottoposti a test cutanei allergologici per gli eccipienti dei vaccini anti COVID-19 e 50 soggetti hanno eseguito il test in vitro BAT. Un solo soggetto ha eseguito i test cutanei tra la prima e la seconda dose e il BAT dopo la terza dose. Gli esiti dei test sono stati negativi per 78 soggetti. Solo 2 casi hanno presentato positività ai test per PEG e polisorbati, venendo esentati dalla vaccinazione sulla scorta del dato clinico e dell’esito dei test. Un paziente ha rifiutato la vaccinazione e 3 soggetti non si sono ripresentati al centro vaccinale. Un numero limitato di soggetti (15 pazienti) ha praticato la vaccinazione frazionata off label con somministrazione di dosi refratte da 0,1 cc a distanza di 30 minuti l'una dall’altra e osservazione per 5 ore dall’ultima dose, alla luce dei test allergologici per gli additivi dei vaccini (3 pazienti con valori borderline per il PEG sono stati ammessi in frazionata) o della valutazione della gravità della reazione alla prima somministrazione del vaccino da parte dello specialista allergologo (8).
Alcuni soggetti con pregressa reazione mucocutanea alla prima dose sono stati premedicati con antistaminico (cetirizina 10 mg) e tenuti in osservazione per 60 minuti. Tutti i pazienti valutati nel centro di secondo livello hanno effettuato vaccinazione controllata in ambito protetto. Non si sono registrate reazioni anafilattiche o, comunque, reazioni riconducibili a reazioni allergiche nella somministrazione della seconda dose. Le modalità di somministrazione sono state ripetute anche per la terza dose.
Il numero di pazienti valutati nel centro di secondo livello per la terza dose risulta inferiore a quello per la seconda dose (5.764 vs 8.134), in quanto i pazienti che hanno eseguito prima e seconda dose senza problemi in ambiente protetto hanno eseguito la terza dose nel centro di primo livello, oltre ad alcuni pazienti esclusi alla terza dose per aver contratto il COVID-19 successivamente alla seconda dose. Non vi sono segnalazioni di eventi avversi alla terza dose, tranne un soggetto giovane di sesso femminile, che presentava test cutanei negativi per gli eccipienti dei vaccini anti COVID-19, eseguiti dopo la prima dose somministrata nel centro di primo livello per sospetta reazione allergica caratterizzata da angioedema del volto con edema linguale a circa 15 minuti dalla somministrazione. Dopo la terza dose la paziente ha ripresentato i medesimi sintomi e segni con simile tempistica, in assenza di sintomi respiratori. La paziente è stata trattata con antistaminico e corticosteroide per via sistemica e il quadro si è risolto dopo 2 ore di osservazione. Ha eseguito successivamente i BAT per gli eccipienti del vaccino presentando positività per PEG 2000 e DMG PEG 2000. In questo caso la reazione di tipo immediata è stata posta in relazione all’additivo del vaccino.
Discussione
L’adozione di un sistema di screening nell’hub di primo livello si è rivelata di primaria importanza per standardizzare l’invio da parte dei medici vaccinatori dei pazienti verso il centro di secondo livello. In tal modo si è presumibilmente contenuto il numero di prestazioni specialistiche richieste, che, comunque, sono risultate numerose considerata la dimensione della campagna vaccinale. Di fatto, alla seconda dose l’1,2% dei soggetti ha avuto accesso alla consulenza specialistica allergologica ed effettuato somministrazione in ambito protetto. Nella seconda dose sono state effettuate le somministrazioni sia ai soggetti che hanno fruito della prima dose in ambito protetto, sia ai soggetti con presunta reazione alla prima dose e, dunque, a uno 0,6% con reazioni che prudenzialmente richiedevano una valutazione e una somministrazione in ambito protetto.
Nel complesso delle reazioni avverse alla vaccinazione non si sono avute reazioni anafilattiche con necessità di interventi di emergenza e/o ricovero ospedaliero. Un solo caso di reazione muco-cutanea immediata è risultato correlato alla sensibilizzazione del PEG 2000, additivo contenuto nel vaccino, a fronte di test cutanei negativi eseguiti dopo la prima dose per reazione immediata. Solo due casi hanno ricevuto un’esenzione dalla vaccinazione. Complessivamente nella casistica riportata nel presente lavoro, il dato di sensibilizzazione/allergia a componenti del vaccino è di rilevanza trascurabile.
Il BAT è ormai uno strumento diagnostico e prognostico dotato di una sempre maggiore accuratezza nei casi di farmaco-allergia e di allergia alimentare, e pertanto si può considerare l’uso del BAT nei soggetti con reazioni alla somministrazione del vaccino (9). I casi con una positività per PEG con valori borderline o debolmente positivi non hanno presentato reazioni con modalità di esecuzione tramite somministrazione frazionata e/o premedicazione con antistaminici. In quattro casi vi è stata discrepanza tra i test cutanei (negativi) e i BAT, ma a fronte di manifestazioni cliniche contenute e di un’anamnesi non indicativa per farmaco-allergia, si è provveduto alla somministrazione frazionata del vaccino. Dalla letteratura si evince, infatti, che la maggioranza dei pazienti con reazioni allergiche ha tollerato una seconda dose sia frazionata sia con premedicazione (10, 11), seguendo le raccomandazioni di completare il ciclo vaccinale in caso di moderate reazioni cutanee o estese reazioni locali (12, 13). Pertanto, le indicazioni di eseguire test allergologici sono state riviste in letteratura e limitate a casi con condizioni di rischio medio-elevato (14). Inoltre, alla luce anche delle esperienze in real-life di un anno di vaccinazioni anti COVID-19, la SIAAIC e l’AAIITO hanno in parte rivalutato il documento pubblicato nel 2021, sottolineando l’opportunità di rivaccinare il paziente con manifestazioni gravi con un vaccino diverso e, in caso di reazioni lievimoderate, valutare il rapporto rischio beneficio ed eventualmente procedere con una premedicazione con antistaminico o una vaccinazione mediante desensibilizzazione o dosi frazionate. L’esecuzione dei test cutanei trova sempre meno indicazioni per un basso valore predittivo positivo e negativo (15) e, in accordo con i dati di letteratura, anche nella nostra esperienza la frequenza di reazioni severe alla seconda dose è assai bassa, in assenza di morti correlate (16). Si sottolinea, pertanto, l’importanza della valutazione medica complessiva effettuata sul paziente, che non deve basarsi solo sull’esito di test allergologici, cutanei o in vitro, ma soprattutto sulla precisa anamnesi allergologica, tenendo conto della severità delle reazioni riportate, in un’ottica di valutazione del rapporto rischio/benefici derivanti dalla vaccinazione (17).
Nel presente studio non vi sono dati a conferma di una maggiore assistenza ai pazienti per uno dei vaccini utilizzati a mRNA, mentre il vaccino ad adenovirus, Vaxzevria ha presentato un maggior numero di eventi avversi alla prima dose. La vaccinazione, come è noto, è stata poi sospesa e passata in eterologa con vaccini a mRNA. Per il Jcovden non abbiamo dati in quanto si è trattato di una mono somministrazione. Non si hanno rilievi per l’ultimo vaccino introdotto, il Nuvaxovid, utilizzato in pochi pazienti.
Conclusioni
Sulla base delle esperienze del centro di secondo livello valutato nel presente lavoro il problema delle reazioni allergiche al vaccino risulta estremamente limitato, anche su pazienti potenzialmente critici in base al dato anamnestico o alla reazione avversa registrata alla prima somministrazione nell’hub vaccinale. Abbiamo, pertanto, potuto così inquadrare molti casi, riportati come reazioni avverse, essere associati ad elementi di natura psicologica ed emotività, stimolati anche da un clima di “fake news” e informazioni distorte dei movimenti no vax. Sicuramente l’esecuzione in un ambito di tranquillità e di assistenza con osservazione prolungata e garanzia di intervento, hanno permesso di affrontare con serenità la vaccinazione. Le reazioni occorse alla prima dose, di cui non molte correttamente o esaustivamente registrate, sono presumibilmente correlate a effetto nocebo della vaccinazione, piuttosto che a una problematica di per sé del vaccino (18), come per altro anche segnalato da altri autori in termini di ansietà e a fattori non immunitari, permettendo così di spiegare le reazioni anafilattiche descritte (19).
Va, infine, sottolineato che le vaccinazioni con virus a mRNA presentano statisticamente un significativo minor numero di effetti avversi rispetto alle vaccinazioni antiinfluenzale ed epatite B (20, 21). L’approccio allergologico, pertanto, deve essere estremamente circoscritto in prospettiva e ben modulato, evitando di ricorrere a un eccesso di valutazioni o di diagnostica. In questa ottica si colloca l’allegato 5 della Direzione sanitaria della Regione Lombardia che illustra in dettaglio tutte le modalità operative che si possono avere e le misure da adottare nei singoli casi/patologie evitando, dunque, un ridondante ricorso alle figure specialistiche e alle strutture di secondo livello. Tale documento può essere visto in un’ottica di evoluzione delle esperienze maturate nei centri di supporto alle vaccinazioni e, in previsioni di nuove campagne vaccinali, sarà uno strumento sicuramente utile (22).
Conflitti di interesse dichiarati: nessuno.
Finanziamenti: nessuno.
Authorship: tutti gli autori hanno contribuito in modo significativo alla realizzazione di questo studio nella forma sottomessa.
Riferimenti bibliografici
- Shimabukuro T, Nair N. Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Pfizer-BioNTech COVID-19 Vaccine. JAMA 2021;325(8):780-1. doi: 10.1001/jama.2021.0600
- Centers for Disease Control and Prevention. Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Moderna COVID-19 Vaccine - United States, December 21, 2020-January 10, 2021. MMWR Morb Mortal Wkly Rep 2021;70:125- 9. doi: 10.15585/mmwr.mn7004e1
- Nilsson L, Brockow K, Alm J, Cardona V, Caubet JC, Gomes E, et al. Vaccination and allergy: EAACI position paper, practical aspects. Pediatr Allergy Immunol 2017;28:628-40. doi 10.1111/pai.12762
- Agenzia Italiana del Farmaco. Rapporto sulla Sorveglianza dei vaccini COVID-19. Rapporto numero 1 - Periodo dal 27/12/2020 al 26/01/2021. www.aifa.gov.it/...; ultimo accesso 23/5/2023.
- Warren CM, Snow TT, Lee AS, Shah MM, Heider A, Blomkalns A, et al. Assessment of Allergic and Anaphylactic Reactions to mRNA COVID-19 Vaccines With Confirmatory Testing in a US Regional Health System. JAMA Netw Open 2021;4(9):e2125524. doi: 10.1001/jamanetworkopen.2021.25524
- Società Italiana di Allergologia, Asma ed Immunologia Clinica. Vaccini per COVID-19: Linee guida per la gestione dei pazienti a rischio di reazioni allergiche. www.siaaic,org/?p=5949; ultimo accesso 23/5/2023.
- Labella M, Céspedes JA, Doña I, Shamji MH, Agache I, Mayorga C, et al. The value of the basophil activation test in the evaluation of patients reporting allergic reactions to the BNT162b2 mRNA COVID-19 vaccine. Allergy 2022;77(7):2067-79. doi: 10.1111/all.15148
- Paoletti G, Racca F, Piona A, Melone G, Merigo M, Puggioni F, et al. Successful SARS-CoV-2 vaccine allergy risk-management: The experience of a large Italian University Hospital. World Allergy Organ J 2021;14(5):100541. doi: 10.1016/j. waojou.2021.100541
- Ebo DG, Elst J, Moonen N, van der Poorten MLM, Van Gasse AL, Garvey LH, et al. Mast cell activation test: A new asset in the investigation of the chlorhexidine cross-sensitization profile. Clin Exp Allergy 2022;52(11):1311-20. doi: 10.1111/ cea.14129
- Antón Gironés M, Montoro Lacomba J, Navarro Cascales T, Lindo Gutarra M, Marco de la Calle FM. Fractional Dosing of the Comirnaty Vaccine in 2 Patients With Immediate Acute Urticaria After the First Dose. J Investig Allergol Clin Immunol 2022;32(2):141-3. doi: 10.18176/jiaci.0717
- Pickert J, Hennighausen I, Mühlenbein S, Möbs C, Pfützner W. Immediate-Type Hypersensitivity to Polyethylene Glycol (PEG) and a PEG-Containing COVID-19 Vaccine Revealed by Intradermal Testing. J Investig Allergol Clin Immunol 2021;31(6):526-27. doi: 10.18176/jiaci.0720
- Krantz MS, Kwah JH, Stone CA, Phillips EJ, Ortega G, Banerji A, et al. Safety Evaluation of the Second Dose of Messenger RNA COVID-19 Vaccines in Patients With Immediate Reactions to the First Dose. JAMA Intern Med 2021;181(11):1530-3. doi: 10.1001/jamainternmed.2021.3779
- Chu DK, Abrams EM, Golden DBK, Blumenthal KG, Wolfson AR, Stone CA, et al. Risk of Second Allergic Reaction to SARS-CoV-2 Vaccines: A Systematic Review and Meta-analysis. JAMA Intern Med 2022;182(4):376-85. doi: 10.1001/ jamainternmed.2021.8515
- Jover Cerdá V, Rodríguez Pacheco R, Doménech Witek J, Alonso Hernández S, Durán García R, Real Panisello M, et al. Allergological study in patients vaccinated against COVID-19 with suspected allergic reactions. Allergy Asthma Clin Immunol 2022;18(1):1-12. doi: 10.1186/s13223-022-00685-z
- Società Italiana di Allergologia, Asma ed Immunologia Clinica. Associazione Allergologi ed Immunologi Italiani Territoriali ed Ospedalieri. Linee di indirizzo per l’inquadramento e la gestione dei pazienti a rischio di reazioni allergiche ai vaccini per il COVID-19. 2022. www.siaaic.org/...; ultimo accesso 23/5/2023.
- Greenhawt M, Abrams EM, Shaker M, Chu DK, Khan D, Akin C, et al. The Risk of Allergic Reaction to SARSCoV- 2 Vaccines and Recommended Evaluation and Management: A Systematic Review, Meta- Analysis, GRADE Assessment, and International Consensus Approach. J Allergy Clin Immunol Pract 2021;9(10):3546-67. doi: 10.1016/j.jaip.2021.06.006
- Cabanillas B, Novak N. Allergy to COVID-19 vaccines: A current update. Allergol Int 2021;70(3):313-8. doi: 10.1016/j.alit.2021.04.003
- Amanzio M, Cipriani GE, Bartoli M. How do nocebo effects in placebo groups of randomized controlled trials provide a possible explicative framework for the COVID-19 pandemic? Expert Rev Clin Pharmacol 2021;14(4):439-44. doi: 10.1080/17512433.2021.1900728
- Csuth À, Nopp A, Storsaeter J, Nilsson L, Jenmalm MC. COVID-19 vaccines and anaphylaxis-evaluation with skin prick testing, basophil activation test and Immunoglobulin E. Clin Exp Allergy 2022;52(6):812-9. doi: 10.1111/ cea.14143
- Cohen SR, Gao DX, Kahn JS, Rosmarin D. Comparison of constitutional and dermatologic side effects between COVID-19 and non- COVID-19 vaccines: Review of a publicly available database of vaccine side effects. J Am Acad Dermatol 2022;86(1):248-9. doi: 10.1016/j. jaad.2021.09.044
- Agenzia Italiana del Farmaco. Rapporto sulla Sorveglianza dei vaccini anti-COVID-19. Periodo dal 27/12/2020 al 26/12/2022 - Rapporto numero 14. www.aifa.gov.it/...; ultimo accesso 23/5/2023.
- Regione Lombardia. Documento di indirizzo per il rilascio delle esenzioni per la vaccinazione anti- COVID-19 febbraio 2022. Protocollo GI 2022.0011094 del 23/2/22022 – All. 5. Welfare DG.; ultimo accesso 23/5/2023.

 Bollettino epidemiologico nazionale
Bollettino epidemiologico nazionale