Tracciabilità e vigilanza in caso di eventi e reazioni avverse gravi segnalate dalle Banche Tessuti italiane dal 2012 al 2024
Liliam Santillia, Monica Vallib, Fiorenza Bariania, Maria Teresa
Vicentinia, Paola Di Ciaccioa, Letizia Lombardinia,
Giovanni Capellib,
Giuseppe Feltrina
aCentro Nazionale Trapianti, Istituto Superiore di Sanità, Roma
bCentro Nazionale per la Prevenzione delle Malattie e la Promozione della Salute, Istituto Superiore di Sanità, Roma
Citare come segue: Santilli L, Valli M, Bariani F, Vicentini MT, Di Ciaccio P, Lombardini L, Capelli G, Feltrin G. Tracciabilità e vigilanza in caso di eventi e reazioni avverse gravi segnalate dalle Banche Tessuti italiane dal 2012 al 2024. Boll Epidemiol Naz 2025;6(1):14-21. DOI: https://doi.org/10.53225/BEN_102
Traceability and surveillance in case of serious adverse events and reactions reported by Italian Tissue Banks from 2012 to 2024
Introduction
The Italian National Transplant Centre (NTC) is a technical structure, which oversees and coordinates tissue procurement, banking and transplantation activities at national level. In accordance with EU Directive 2004/23/ EC, EU technical Directives 2006/17/EC and 2016/86/EC, all Member States have designated an authority, responsible for receiving and managing serious adverse reaction event (SAREs) notifications in the tissue sector. NTC activities in this field also include the annual data collection on tissue donation, transplantation and banking, as well as the management of a vigilance system on epidemiological issues. The aim of this paper is to present an overview of the data on the notifications collected between 2012 and 2024 to assess the trend over the years. It also provides a detailed analysis of the 2023-2024 data, which is most representative of the current context.
Materials and methods
This study is a retrospective analysis of notifications on SAREs reported at national level by the Italian Tissue Banks (TBs) from 2012 to 2024, divided by year and kind of tissues, with a more in-depth analysis on the most updated data relating to the last two years, 2023 and 2024. A procedure for the correct notification of SAREs has been sent to all TBs, together with the reporting forms, according to the Italian legislation. TBs must notify the Regional Authority and to the NTC whenever a SARE is even just suspected. The NTC receives the notifications, assists the centers in managing and solving the problems, and provides the European Commission with all the information on the SAREs received in the previous year.
Results
A total of 196 SAREs were reported in relation to tissue donation and transplantation. The analysis reveals a generally stable trend over the years. In the most recent biennium, 15 SAREs were reported in 2023 and 13 in 2024, highlighting a consistently low notification rate in the context of increasing donation and transplantation activity. Specifically, in 2023, the reported reactions mainly involved corneal tissues for Serious Adverse Event (SAE) and musculoskeletal tissues for Serious Adverse Reaction (SAR), in line with the distribution of donation activity. With regard to 2024, SAE notifications involved corneal tissues, cardiac tissues, and skin tissues, while one SAR was associated with vascular tissue.
Discussion and conclusions
Our analysis highlights how a steady management of SAREs strengthens organization and activity governance and it fosters positive synergies among specialists, therefore playing a major role for network development. The low rate of notifications vs activity volumes suggests however that there is still some room for vigilance improvement.
Key words: tissue bank; serious adverse events and reactions; vigilance
Introduzione
Il Centro Nazionale Trapianti (CNT) è un organismo tecnico che svolge funzioni di indirizzo, coordinamento, sorveglianza e promozione delle attività relative alla donazione e al trapianto di organi, tessuti e cellule destinati ad applicazioni sull’uomo (1, 2).
Il trapianto di tessuti, al pari di quello degli organi e delle cellule, ha una grande importanza in termini di salute pubblica, rappresentando in alcuni casi una terapia salvavita (come per le valvole cardiache) e in altri una soluzione terapeutica che consente un miglioramento della qualità della vita (come per le cornee). Nella maggior parte dei casi i tessuti vengono prelevati da donatori deceduti, ma in alcune situazioni, come negli interventi medici pianificati (ad esempio, interventi ortopedici), possono provenire da donatori viventi. I tessuti vengono conservati nelle banche dei tessuti (BT) - diversamente dagli organi che devono essere trapiantati immediatamente - e, in base alla tipologia di tessuto, la conservazione può andare da pochi giorni ad alcuni anni, permettendo una maggiore flessibilità per il trapianto (3). Inoltre, a differenza degli organi, non vi è carenza di tessuti e non esiste una lista di attesa nazionale, poiché ogni BT ha la propria lista di attesa gestita a livello regionale.
Le BT sono strutture sanitarie pubbliche autorizzate a raccogliere, selezionare, conservare, processare e distribuire tessuti umani a scopo di trapianto sul territorio italiano, garantendo la tracciabilità, la qualità, l’idoneità del donatore e la sicurezza dei prodotti. Attualmente, in Italia, abbiamo 30 BT per le diverse tipologie di tessuti e più precisamente 15 BT mono-tessuto e 15 BT multi-tessuto (4, 5).
In ambito legislativo, l'Unione Europea, attraverso specifiche direttive, ha operato per definire un quadro normativo comune per ciascun Stato membro, influenzando in modo significativo le attività regolatorie relative alla qualità e alla sicurezza richieste per tutte le fasi e le attività legate al settore dei tessuti, nonché per garantire un elevato livello di protezione della salute umana (6-10).
Le normative di riferimento, a livello nazionale, designano il Ministero della Salute e le Regioni, nei rispettivi ambiti di competenza, come autorità responsabili dell’attuazione delle disposizioni sulla sorveglianza dei criteri di qualità e sicurezza dei tessuti, attività che svolgono avvalendosi del supporto del CNT (6-9, 11).
Il CNT coordina e interagisce con le realtà regionali (Centri di Coordinamento Regionale, CRT) e locali (BT, ospedali, centri trapianto, ecc.) per gestire tali attività (1, 2).
Tra le misure riguardanti la qualità e la sicurezza dei tessuti, è prevista la gestione e notifica di eventi e reazioni avverse gravi (REAG): un evento avverso grave (EAG) si configura come un evento negativo imprevisto connesso a qualsiasi fase del processo di donazione e trapianto di tessuti; una reazione avversa grave (RAG) è una risposta non voluta, nel donatore o nel ricevente che si manifesta nella fase di approvvigionamento o applicazione di tessuti (6-9, 11). Nel complesso, le RAG riguardano problematiche che coinvolgono i donatori e i riceventi, mentre le EAG si riferiscono alle complicazioni legate al processo e ai tessuti.
Il CNT riceve e gestisce le notifiche obbligatorie dei REAG inviate dalle BT mediante la specifica modulistica (11), i referenti del settore tessuti del CNT eseguono la valutazione della gravità/severità dell’evento o della reazione notificata, dalla quale possono emergere eventuali provvedimenti da intraprendere.
L’obiettivo di questo lavoro è presentare una panoramica sui dati relativi alle notifiche raccolte tra il 2012 e il 2024 per valutare l’evoluzione temporale del trend negli anni, fornendo anche un’analisi dettagliata dei dati riferiti al biennio 2023-2024 più rappresentativi del contesto attuale.
Materiali e metodi
Lo studio è di tipo retrospettivo e si basa sull’analisi dei dati raccolti nel contesto della sorveglianza nazionale dei REAG.
In linea con la norma ISO 9001, l’area sanitaria Tessuti del CNT raccoglie, archivia e registra tutta l’attività inerente i REAG, garantendo la trasparenza dell’intero processo nelle BT.
I REAG possono verificarsi in qualunque momento, dall’identificazione del donatore fino al trapianto e il riscontro può giungere da qualunque struttura coinvolta nelle diverse fasi del percorso.
La tracciabilità del percorso tra donatore e ricevente, e viceversa, riveste un ruolo fondamentale nel sistema di qualità e sicurezza della Rete Trapianti dei Tessuti. Questa Rete, strutturata su diversi livelli organizzativi, coinvolge a vario titolo non solo le BT, ma anche i CRT e, in ambito locale, gli ospedali, i Centri prelievo, i Centri trapianto al fine di gestire in modo centralizzato le attività inerenti alla donazione, raccolta, lavorazione e conservazione dei tessuti e ai trapianti (1, 2). In questo contesto, la tracciabilità consente di risalire rapidamente dal donatore al ricevente in caso di un REAG, permettendo un intervento tempestivo qualora si presentino problematiche correlate.
Quindi, le BT, oltre all’obbligo di inviare le notifiche dei REAG, devono fornire chiare istruzioni operative a tutti i Centri trapianto, ai Centri Prelievo e alle altre strutture coinvolte. A tal fine, è stata elaborata una procedura operativa standard (POS) per la notifica rapida, da inviare al CNT e al CRT, distribuita a tutte le BT (Materiale Aggiuntivo - Tabella 1) (11). Inoltre, qualora i REAG dovessero riguardare le donazioni multi-organo e multi-tessuto, la comunicazione al CNT relativa ai tessuti potrà essere notificata anche dai CRT tramite il Sistema informativo Trapianti (1, 2) del CNT (Figura 1).
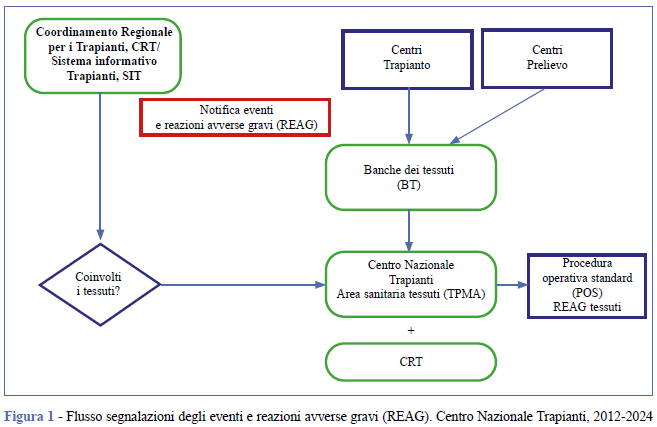
Le informazioni raccolte vengono analizzate mediante l’utilizzo di strumenti di valutazione del rischio e scale di valutazione per classificarle (Materiale Aggiuntivo- Tabella 2) (11), che consentono di misurare il livello di gravità e la probabilità di ripetizione dei REAG, al fine di definire se sia necessario un intervento o se l’indagine effettuata dalla stessa BT sia completa.
Pertanto, a seguito della valutazione della notifica, l’area sanitaria tessuti deciderà gli eventuali provvedimenti da intraprendere, che potrebbero essere così schematizzati:
- valutazione della completezza delle schede e, se necessario, la richiesta di ulteriori informazioni al CRT/BT;
- decisione di pianificare un’ispezione urgente;
- comunicazione dell'evento agli altri possibili soggetti coinvolti.
In ogni caso, le segnalazioni ricevute devono includere tutte le informazioni pertinenti disponibili e i risultati delle indagini in modo da determinarne le cause.
Inoltre, ogni BT deve disporre a sua volta di una POS che consenta il rapido ritiro dalla distribuzione di qualsiasi prodotto che possa essere associato ai REAG. Ogni anno, la Commissione Europea (CE) richiede a tutti gli Stati membri di compilare un form per la comunicazione dei REAG ricevuti nel corso dell’anno precedente (12). L’area sanitaria tessuti del CNT compila annualmente il modulo e, in accordo con il Ministero della Salute, provvede all'invio telematico. Successivamente, la CE pubblica un report annuale con le segnalazioni ricevute da ogni Paese, suddivise per tipologia di tessuto e classificate per fase del processo e tipo di evento/reazione (12).
Nel presente studio l’analisi è stata effettuata sul numero di segnalazioni di REAG e le tipologie di tessuti coinvolti negli ultimi 13 anni, con un’attenzione particolare ai dati più recenti, riferiti al biennio 2023-2024, in relazione alle fasi del processo interessate.
I dati relativi alle notifiche ricevute dal CNT sono stati elaborati utilizzando il programma Microsoft Excel. Le differenze nelle incidenze dei REAG tra i gruppi sono state analizzate mediante Test di Fisher. Le analisi statistiche sono state effettuate utilizzando il software STATA12, considerando un valore di p< 0,05 come soglia di significatività.
Risultati
Nel periodo 2012-2024, il CNT ha ricevuto 196 notifiche di REAG, comprendenti 158 EAG e 38 RAG, per le diverse tipologie di tessuti: cornee, muscoloscheletrico, vasi, cute, membrana amniotica, valvole, isole pancreatiche e tessuto paratiroideo. Considerando il totale delle segnalazioni, le RAG corrispondono al 19% e le EAG all’81%.
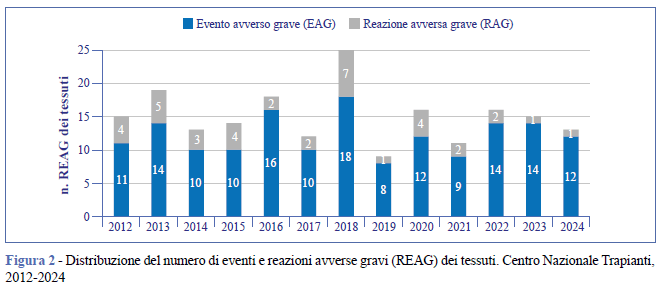
Nella Figura 2 sono riportati i dati sopra descritti da cui si evince come il trend si confermi sostanzialmente stabile negli anni con un numero relativamente contenuto di notifiche, soprattutto nel 2019 (EAG n. 8; RAG n. 1), a eccezione del 2018. In quest’ultimo si è registrato, infatti, il maggior numero di segnalazioni (EAG n. 18; RAG n. 7), nonostante il numero delle BT presenti sul territorio nazionale non abbia avuto variazioni significative negli anni e il trend di donazioni e trapianti sia rimasto piuttosto uniforme.
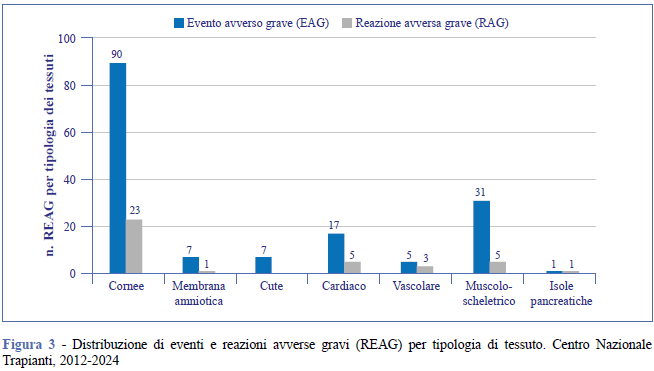
Analizzando nello specifico le tipologie di tessuti coinvolte, nelle 196 notifiche pervenute al CNT il maggior numero di notifiche ha riguardato le cornee, tessuto maggiormente donato, con 90 EAG (57%) e 23 RAG (60%); per gli altri tessuti sono stati riportati: 7 EAG (4.4%) e 1 RAG (2,6%) membrana amniotica; 7 EAG (4,4%) e nessuna RAG cute; 17 EAG (11%) e 5 RAG (13%) cardiaco; 5 EAG (3%) e 3 RAG (8%) vascolare; 31 EAG (19,6%) e 5 RAG (13%) TMS e, infine, le isole pancreatiche con 1 EAG (0,6%) e 1 RAG (2,6%) (Figura 3).
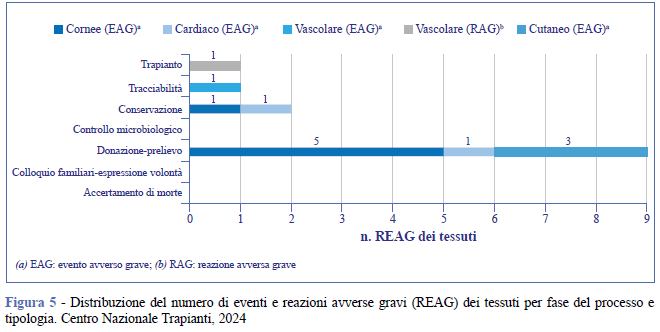
Per quanto riguarda l’analisi dei dati più recenti disponibili (2023 e 2024), nel 2023 sono stati notificati al CNT 15 REAG, di cui 14 EAG e 1 RAG (4), mentre nel 2024 sono stati notificati 13 REAG, di cui 12 EAG e 1 RAG. In conformità con il modello standard CE, i REAG ricevuti sono stati analizzati, per ciscun tipo di tessuto, secondo le diverse fasi del processo a cui si riferiscono (dall’identificazione del donatore fino al trapianto dei tessuti), come illustrato nelle Figure 4 e Figura 5: accertamento di morte, colloquio con i familiari, espressione di volontà, donazione e prelievo, approvvigionamento, lavorazione, controlli microbiologici, conservazione, selezione del prodotto, rilascio, distribuzione, tracciabilità e trapianto.
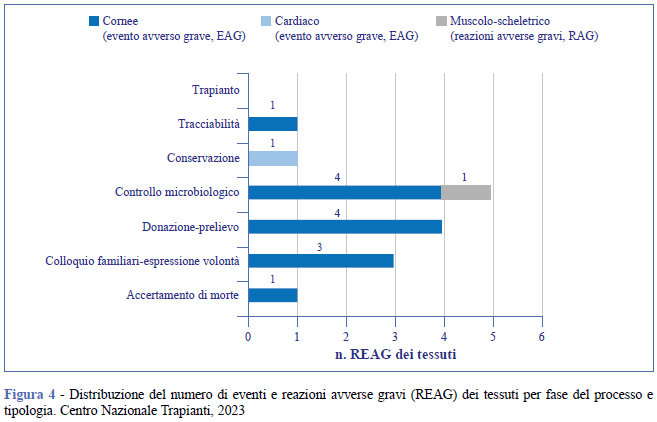
Nello specifico, in merito al 2023 (Figura 4), 13 EAG erano legati alle cornee e riguardavano le fasi di: accertamento di morte, colloquio con i familiari, espressione della volontà, donazione e prelievo dei tessuti, controllo microbiologico e tracciabilità; 1 EAG, invece, era riferito al tessuto cardiaco, in particolare alla fase di conservazione. Per quanto riguarda la RAG, questa è associata al tessuto muscolo-scheletrico, con riferimento al controllo microbiologico (4). In particolare, è stata necessaria la rimozione del tessuto a causa del verificarsi di una infezione batterica post trapianto.
Per quanto riguarda invece il 2024 (Figura 5), 6 EAG sono legati alle cornee e riguardano le fasi di donazione/prelievo e conservazione; 2 EAG sono relativi al tessuto cardiaco, nelle fasi di donazione/prelievo e conservazione, e 3 EAG interessano il tessuto cutaneo nella fase di donazione/prelievo. Per il tessuto vascolare, 1 EAG è legato al processo della tracciabilità e 1 RAG alla fase del trapianto. Nello specifico la RAG si è verificata a causa del mancato attecchimento del tessuto dovuto allo stato infettivo microbico del ricevente. La Tabella riporta i tessuti interessati ai REAG e le incidenze calcolate per ciascuna tipologia di tessuto corrispondente, sia riferiti all’anno 2023 che all’anno 2024.
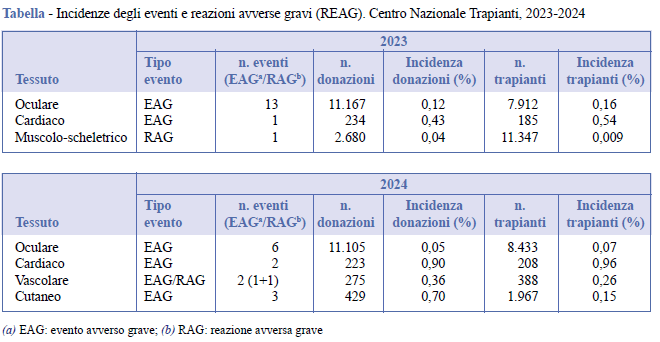
Per quanto riguarda il confronto tra questi due anni, l’analisi statistica delle incidenze di EAG, relativi alle donazioni e ai trapianti di tessuti oculari e cardiaci, non ha evidenziato differenze statisticamente significative. Nel caso del tessuto oculare, l’incidenza di EAG per donazione è passata da 0,12% nel 2023 a 0,05% nel 2024, ma tale riduzione non ha raggiunto la significatività statistica (p = 0,167). Analogamente, anche per i trapianti oculari, la diminuzione dell’incidenza da 0,16% a 0,07% non è risultata statisticamente significativa (p = 0,107). Per quanto riguarda il tessuto cardiaco, le differenze osservate tra i due anni sono risultate anch’esse non significative, sia per le donazioni (p = 0,615) sia per i trapianti (p = 1,000). Questi risultati indicano una sostanziale stabilità delle incidenze di EAG nei due anni considerati per i tessuti analizzati.
Discussione e conclusioni
La segnalazione di REAG al CNT riveste un ruolo fondamentale poiché, da un lato, protegge sia i pazienti che gli operatori in situazioni come contaminazioni, infezioni o utilizzo di materiali potenzialmente difettosi, consentendo un rapido ritiro anche di eventuali tessuti stoccati e non ancora distribuiti; dall’altro, favorisce lo scambio e la condivisione di informazioni tra i professionisti del settore, contribuendo a una migliore comprensione del sistema e alla diffusione di buone pratiche.
La vigilanza, nella gestione degli REAG, è fortemente connessa con la tracciabilità ed è necessaria affinché si abbia:
- la possibilità di ricostruire il percorso dei tessuti in ogni fase dell'approvvigionamento, della lavorazione, del controllo e dello stoccaggio fino alla distribuzione al ricevente o allo smaltimento;
- la possibilità di risalire all'identificazione del donatore, della BT o del centro di produzione che riceve o lavora o stocca i tessuti;
- la possibilità di individuare i responsabili che applicano i tessuti sui riceventi a livello delle strutture sanitarie.
In 13 anni sono state registrate 196 REAG riguardo donazione e trapianti di tessuti e, dall'analisi dei REAG pervenuti al CNT nel periodo 2012-2024, si evidenzia un andamento uniforme sul numero di notifiche registrate, tranne per l’anno 2018, in cui emerge una maggior percentuale sia di EAG che di RAG ricevute.
Nel 2023 si evince come il numero delle notifiche (15 REAG) risulti basso se confrontato con l'attività di donazione e trapianto di tessuti, che nel 2023 ha registrato 15.327 donazioni e 24.944 trapianti (4).
Inoltre, nel corso dell'anno 2023, emerge che la RAG è legata al tessuto muscolo-scheletrico, mentre le segnalazioni relative a EAG riguardano prevalentemente problematiche connesse ai tessuti corneali, che sono il tipo di tessuto con il maggior numero di attività di donazione (11.167 donazioni nel 2023 su un totale di 15.327 donatori) (4).
Anche per l’anno 2024 il numero delle notifiche (13 REAG) risulta essere ancora basso se confrontato con l’attività di donazione e trapianto di tessuti, che nel 2024 ha registrato più donazioni e trapianti rispetto al 2023: 15.487 donazioni e 25.872 trapianti.
Analizzando gli ultimi due anni, la frequenza dei REAG nel complesso risulta piuttosto bassa come presentato nella Tabella, dove sono riportate le basse percentuali di incidenza per le diverse tipologie di tessuti.
Le tipologie di eventi più frequenti hanno riguardato il tessuto corneale e le fasi del processo maggiormente coinvolte sono la fase di donazione-prelievo, controllo microbiologico, colloquio familiari-espressione di volontà.
In riferimento al contesto europeo, è stato possibile confrontare con gli altri Paesi europei solo i dati relativi all’anno 2023, i più recenti disponibili (12). Nel 2023 sono stati segnalati complessivamente 187 EAG e 42 RAG associati all'impiego di tessuti umani, provenienti da 31 Paesi. I tessuti maggiormente coinvolti risultano essere quelli muscolo-scheletrici e oculari, in linea con le tendenze osservate anche negli anni precedenti. Rispetto al panorama europeo, l’Italia presenta un numero relativamente contenuto di segnalazioni. Sebbene le modalità di classificazione possano variare tra i diversi Paesi, il confronto indica un tasso di incidenza in Italia inferiore alla media europea, a conferma della solidità del sistema nazionale di vigilanza e tracciabilità dei tessuti. Tuttavia, la possibile sottosegnalazione a livello europeo rende necessaria una cauta interpretazione comparativa dei dati.
In ambito di vigilanza, oltre all’obbligo di notifica a livello nazionale, nel caso in cui i REAG riguardino tessuti che possono essere utilizzati tra Paesi europei, esiste anche l’obbligo di notificare tempestivamente a livello europeo le allerte rapide relative a tessuti e cellule (Rapid Allert Tessues and Cells-RATC), tramite una piattaforma dedicata (13). Su questa piattaforma le autorità competenti di ogni Paese caricano le allerte che coinvolgono due o più Stati. L’obiettivo è garantire un sistema che notifichi tempestivamente i Paesi interessati ogniqualvolta si verifichi un evento che richiede un intervento urgente o azioni precauzionali per affrontare un potenziale rischio grave per la salute pubblica legato all’utilizzo di tessuti. Alcuni esempi di allerte rapide che possono essere inserite nella piattaforma includono:
- difetti di qualità e/o sicurezza riguardanti specifici tessuti;
- attività illegali e fraudolente;
- evoluzione di situazioni rapide e/o significative di tipo epidemiologico;
- notifiche (richiami, misure preventive, raccomandazioni, ecc.) da altri settori della sanità (ad esempio, dispositivi medici, sangue e prodotti derivati, medicinali, organi). Il sistema è tuttora operativo e lo scambio di informazioni tra i vari Paesi si è rivelato estremamente utile (14, 15).
In conclusione, nel lavoro qui presentato si osserva che nel complesso il numero di notifiche di REAG al CNT è rimasto sostanzialmente stabile negli anni. L’utilizzo di procedure operative chiare e ben definite, la continuità del programma ispettivo sulla vigilanza, nonché una comunicazione più fluida e diretta, hanno contribuito a rendere più efficace ed efficiente il funzionamento dell'intera rete dei tessuti, aumentando consapevolezza e rafforzando il rapporto di fiducia tra tutti i soggetti coinvolti. Tuttavia, il basso tasso di notifiche ricevute rispetto ai volumi di attività registrati suggerisce che ci siano ancora margini di miglioramento in termini di tracciabilità e vigilanza nella gestione dei REAG. Pertanto, lo strumento formativo rivolto agli operatori delle BT, centrato sulla valutazione del rischio, si conferma fondamentale per accrescere ulteriormente la consapevolezza sulla corretta gestione dei REAG, comprese le segnalazioni, per migliorare e aumentare la sicurezza dell’intero processo.
Conflitti di interesse dichiarati: nessuno.
Finanziamenti: nessuno.
Authorship: tutti gli autori hanno contribuito in modo significativo alla realizzazione di questo studio nella forma sottomessa.
Riferimenti bibliografici
- Domini F, Vespasiano F, Di Ciaccio P, Lombardini L, Cardillo M. Trasparenza, efficacia ed efficienza della Rete Nazionale Trapianti dalla sua nascita ai giorni nostri: evoluzione di un modello organizzativo al servizio del paziente affetto da grave insufficienza di organo. Boll Epidemiol Naz 2023;4(3):27-34; doi: 10.53225/BEN_072
- Ministero della Salute, Istituto Superiore di Sanità, Centro Nazionale Trapianti. Trapianti. www.trapianti.salute.gov.it...; ultimo accesso 26/6/2025.
- European Directorate for the Quality of Medicines & HealthCare. Tissue donation - Everything you need to know. Council of Europe 2022. www.edqm.eu... ; ultimo accesso 26/6/2025.
- Centro Nazionale Trapianti, Istituto Superiore di Sanità. Report 2023. Attività Annuale Rete Nazionale Trapianti. Ultimo aggiornamento maggio 2025. www.trapianti.salute.gov.it...; ultimo accesso 26/6/2025.
- Ministero della Salute, Istituto Superiore di Sanità, Centro Nazionale Trapianti. Trapianti. Ultimo aggiornamento maggio 2025. www.trapianti.salute.gov.it...; ultimo accesso 26/6/2025.
- Italia. Decreto Legislativo 6 novembre 2007, n. 191. Attuazione della direttiva 2004/23/CE sulla definizione delle norme di qualità e di sicurezza per la donazione, l'approvvigionamento, il controllo, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umani. Gazzetta Ufficiale - Serie Generale n. 261 del 9 novembre 2007 - Suppl. Ordinario n. 228.
- Italia. Decreto Legislativo 25 gennaio 2010, n. 16. Attuazione delle direttive 2006/17/CE e 2006/86/ CE, che attuano la direttiva 2004/23/ CE per quanto riguarda le prescrizioni tecniche per la donazione, l'approvvigionamento e il controllo di tessuti e cellule umani, nonché per quanto riguarda le prescrizioni in tema di rintracciabilità, la notifica di reazioni ed eventi avversi gravi e determinate pre-scrizioni tecniche per la codifica, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umani. Gazzetta Ufficiale - Serie Generale n. 40 del 18 febbraio 2010.
- Italia. Decreto Legislativo 30 maggio 2012, n. 85. Modifiche ed integrazioni al decreto legislativo 25 gennaio 2010, n. 16, recante attuazione delle direttive 2006/17/CE e 2006/86/CE, che attuano la direttiva 2004/23/CE per quanto riguarda le prescrizioni tecniche per la donazione, l'approvvigionamento e il controllo di tessuti e cellule umani, nonché per quanto riguarda le prescrizioni in tema di rintracciabilità, la notifica di reazioni ed eventi avversi gravi e determinate prescrizioni tecniche per la codifica, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umani. Gazzetta Ufficiale - Serie Generale n. 147 del 26 giugno 2012 - Suppl. Ordinario n. 130.
- Italia. Decreto Legislativo 16 dicembre 2016, n. 256. Attuazione della direttiva 2015/565/UE che modifica la direttiva 2006/86/CE per quanto riguarda determinate prescrizioni tecniche relative alla codifica di tessuti e cellule umani. Gazzetta Ufficiale - Serie Generale n. 10 del 13 gennaio 2017.
- Navarro A, Len O, Muñiz-Diaz E, Vives Corrons JL, Dominguez-Gil B, Vilarrodona A, et al. The value of organ and tissue biovigilance: a cross-sectional analysis. Front Transplant 2024;3:1307946. doi: 10.3389/frtra.2024.1307946
- Accordo, ai sensi dell’articolo 6, comma 1, del decreto legislativo 6 novembre 2007, n.191, tra il Governo, le Regioni, le Province autonome di Trento e Bolzano sul documento recante “Requisiti minimi organizzativi, strutturali e tecnologici degli Istituti dei tessuti per la qualità e la sicurezza nella donazione, l’approvvigionamento, il controllo, la lavorazione, la conservazione, lo stoccaggio e la distribuzione di tessuti e cellule umane”. Rep. Atti n. 66/CSR seduta 8 marzo 2018.
- European Commission. Annual SARE Report 2024. Tissues and Cells. (Data collected from 01/01/2023 to 31/12/2023 and submitted to the European Commission in 2024). www.notifylibrary.org...; ultimo accesso 7/7/2025.
- European Commission. Rapid Alert system for human Tissues and Cells (RATC) and for human Blood and Blood Components (RAB). Summary of 2024 activities. Ref. Ares(2025)542703 - 23/1/2025. health.ec.europa.eu...; ultimo accesso 26/6/2025.
- Fehily D, Sullivan S, Noel L, Harkin D. Improving Vigilance and Surveillance for Tissues and Cells in the European Union: EUSTITE, SOHO V&S and Project NOTIFY. Organs, Tissues and Cells 2012;15(2):85-95.
- Len O, Greenwald MA, Navarro A, Petrisli E, Carella C, Grossi PA, et al. Perspectives on donor-derived infections from the Notify Library. Transpl Infect Dis 2024;26 Suppl 1:e14359. doi: 10.1111/ tid.14359.

 Bollettino epidemiologico nazionale
Bollettino epidemiologico nazionale