Aspetti clinici e possibili complicanze
Il periodo di incubazione va dai 3 ai 14 giorni, mentre il periodo medio di incubazione è di 4-7 giorni [1]. L’infezione può essere asintomatica in più del 50% dei casi o caratterizzata da una malattia febbrile moderata, la cosiddetta febbre da Dengue (DF, Dengue Fever), fino ad arrivare, in circa il 5% dei casi sintomatici, alle forme più gravi della febbre Dengue emorragica (DHF, Dengue Hemorrhagic Fever) e della sindrome da shock per dengue (DSS, Dengue Shock Syndrome).
Secondo la classificazione in livelli di gravità stilata dall’Organizzazione Mondiale della Sanità (OMS) nel 1997, la DHF è stata ulteriormente suddivisa in quattro stadi di gravità, con il III e IV definiti come DSS che rappresenta la sindrome clinica più grave, caratterizzata da anomalie nella coagulazione, perdita di plasma e aumento della fragilità vascolare. Il deficit di liquidi, dovuto all’aumento della permeabilità capillare, porta a shock ipovolemico e insufficienza multiorgano [2]. La DHF e la DSS rappresentano una delle principali cause di ospedalizzazione e morte tra i bambini e gli adulti nelle aree dove l’infezione è endemica. La sopravvivenza, nel caso delle forme più gravi, dipende dalla possibilità di avere accesso ad adeguate terapie di supporto e a un continuo monitoraggio dell’evoluzione delle condizioni del paziente. Il tasso di mortalità può infatti variare da meno dell’1% fino a circa il 10-15% a seconda della presenza o meno di cure [3].
Le difficoltà nell’applicare nella clinica i criteri che definivano la DHF, insieme all'aumento dei casi gravi di malattia che non soddisfacevano i suddetti criteri, hanno portato a una rivalutazione della precedente classificazione dell’OMS, sebbene la suddivisione in DF/DHF/DSS continui ad essere ampiamente utilizzata.
Nel 2009 la categorizzazione in livelli di gravità dei casi di malattia sintomatica da DENV è stata riveduta in “con” o “senza” segnali d’allarme e dengue severa. Rappresentano casi probabili di infezione senza segnali di allarme, quelli costituiti dai pazienti sintomatici che hanno recentemente viaggiato in aree endemiche per l’infezione (o che vivono normalmente in queste aree), che presentano febbre e due tra i seguenti sintomi: nausea o vomito, rash, dolore (tra cui dolore retrobulbare e/o altri sintomi oculari) [1, 4], positività al test di fragilità capillare e leucopenia. I pazienti con le caratteristiche e i sintomi descritti e che poi risultino positivi a un test di laboratorio per l’infezione, possono presentare dei segnali di allarme, tra cui dolore addominale, vomito persistente, accumulo clinicamente rilevante di liquidi (asciti e versamenti pleurici), sanguinamento delle mucose, letargia e irrequietezza, ingrossamento del fegato >2 cm (epatomegalia) e aumento dell’ematocrito in concomitanza con una rapida diminuzione nella conta piastrinica, che richiedono un’osservazione rigorosa ed assistenza medica. Anche i pazienti inizialmente senza segnali d’allarme possono progredire verso la dengue severa, mentre non tutti quelli con segnali d’allarme progrediscono verso la malattia grave.
La Dengue severa è invece associata a tre condizioni cliniche:
- una grave perdita di plasma verso i tessuti circostanti, dovuta a un aumento della permeabilità capillare, che porta allo shock per Dengue e all’accumulo di fluidi associato a distress respiratorio
- un sanguinamento grave
- un grave interessamento degli organi tra cui il fegato, con valori degli enzimi epatici (AST o ALT) >1000 U/l, il sistema nervoso centrale (SNC) con alterazione dello stato di coscienza, il cuore con sviluppo di miocardite, ed altri organi (vedi figura).
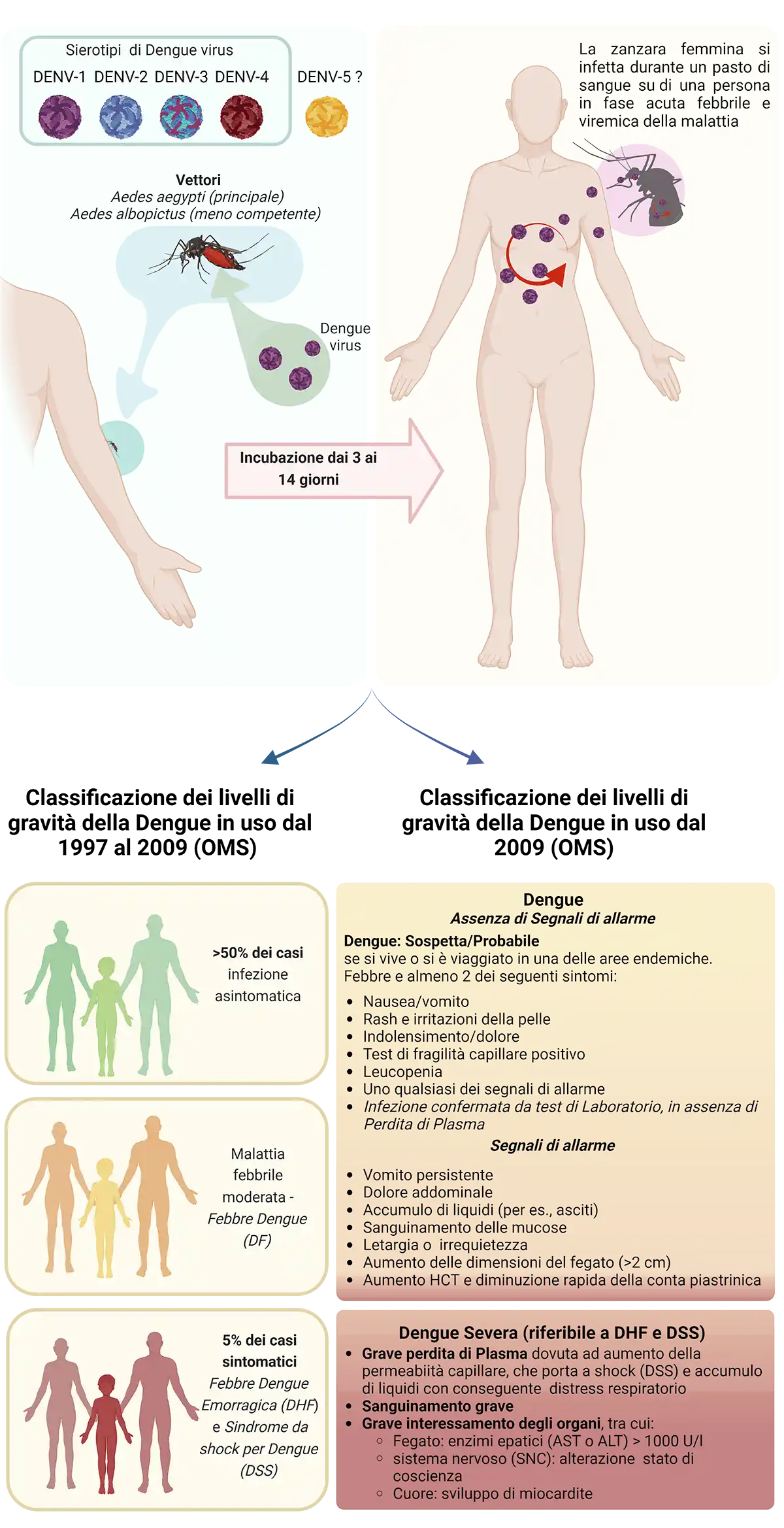
Figura: Il virus Dengue è costituito da 4 sierotipi diversi (DENV-1, -2, -3 e –4) ciascuno dei quali presenta genotipi distinti seppur altamente correlati nella sequenza nucleotidica del loro RNA genomico, La scoperta di un possibile quinto sierotipo (DENV-5) è stata riportata una sola volta nel 2015. Dopo un periodo di incubazione che va dai 3 ai 14 giorni dall’infezione da parte di una zanzara femmina infetta (generalmente Aedes aegypti) si possono avere diversi gradi di gravità di malattia che vanno da un’infezione asintomatica o paucisintomatica ad una malattia severa ad esito potenzialmente fatale, come descritto dai livelli di classificazione di gravità dell’OMS. (Creata da Giorgia Napoletani e Marco Sgarbanti con BioRender.com).
I bambini corrono un rischio maggiore di sviluppare una forma grave di malattia in quanto meno capaci degli adulti di compensare le perdite di plasma a livello dei capillari e di conseguenza maggiormente a rischio di DSS.
L’identificazione di marcatori per la gravità della malattia, o per un aumentato rischio di progressione verso le forme più severe, è di grande interesse per la ricerca sulla Dengue. La maggior parte degli studi sono stati rivolti ai marcatori immunologici di Dengue grave che includono diverse citochine, tra cui le interleuchine (IL)-7, -8, e -10, il fattore di crescita trasformante (TGF)-β, il fattore di necrosi tumorale (TNF)-α, e l’interferone (IFN)-g. Gli elevati livelli di citochine nella Dengue grave costituiscono un importante fattore predittivo della gravità dell’infezione; inoltre, i livelli di eparan solfato nelle urine sono risultati significativamente aumentati nei bambini con DSS, così come i livelli plasmatici di pentraxina 3, una proteina della fase acuta, rispetto ai livelli plasmatici di albumina che invece risultano diminuiti [5]. I livelli del fattore di crescita dell’endotelio vascolare (VEGF) risultano significativamente elevati nei pazienti con DHF rispetto a quelli dei pazienti con DF o del gruppo di controllo. Inoltre, i livelli della molecola di adesione cellulare vascolare (VCAM)-1, che evidenzia uno stato di attivazione delle cellule endoteliali, sono risultati significativamente elevati nei pazienti DSS rispetto a quelli dei pazienti DF. Infine, alti livelli di inibitore dell'attivatore del plasminogeno di tipo 1, al momento del ricovero, sono stati associati ad un esito fatale [5].
Le infezioni responsabili delle diverse forme di malattia sopradescritte sono causate da virus appartenenti ai quattro diversi sierotipi che vanno da DENV-1 a DENV-4, e che quindi sono stati caratterizzati in base alle loro diverse interazioni con gli anticorpi presenti nel siero dei pazienti. Ciascuno dei diversi sierotipi si presenta con genotipi distinti seppur altamente correlati nella sequenza nucleotidica del loro RNA genomico, evidenziando nel complesso l'ampia variabilità genetica di questo virus. La scoperta di un possibile quinto sierotipo (DENV-5) è stata riportata nel 2015 [6].
Le persone che si infettano per la prima volta con DENV sono protette dallo sviluppo di malattia da reinfezione con lo stesso ceppo virale e, limitatamente ai 2-3 mesi successivi alla prima infezione, anche dalla reinfezione con un sierotipo diverso (cross-protezione o immunità eterotipica). Questi soggetti sono anche protetti dalla malattia grave per circa 2 anni, ma non a lungo termine [2].
Pur permanendo per tutta la vita la protezione contro il sierotipo responsabile della prima infezione (immunità omotipica), un’infezione successiva con un sierotipo diverso può verificarsi dopo un periodo iniziale di cross-protezione e, se il periodo fra le infezioni con sierotipi diversi è particolarmente lungo (maggiore di 2 anni), possono manifestarsi le forme di malattia più severe a causa del fenomeno ADE (antibody dependent enhancement/potenziamento anticorpo-dipendente)). Casi gravi possono verificarsi anche in seguito a infezioni primarie ma sono rari mentre le terze o quarte infezioni sono generalmente asintomatiche o caratterizzate da sintomi lievi [1]. In particolare, la sintomatologia dell’infezione primaria da DENV è maggiore all’aumentare dell’età, in particolare negli anziani o in pazienti con malattie croniche, come il diabete mellito, la broncopneumopatia cronica ostruttiva (BPCO) o le malattie cardiovascolari [1]. Per quanto riguarda invece le infezioni secondarie, il rischio di progredire verso la DHF e la DSS è di circa 5 volte inferiore negli adulti rispetto ai bambini come dimostrato in una popolazione di età maggiore o uguale ai 3 anni, esposta a uguali tassi di infezioni secondarie con DENV-2 [1].
Riferimenti
- Guzman, M.G., Gubler, D.J., Izquierdo, A., Martinez, E., Halstead, S.B., 2016. Dengue infection. Nat. Rev. Dis. Prim. 2, 16055. DOI: 10.1038/nrdp.2016.55
- OMS “Dengue guidelines, for diagnosis, treatment, prevention and control”
- Palanichamy Kala M., St John A.L., Rathore A.P.S. Dengue: update on clinically relevant therapeutic strategies and vaccines. Curr Treat Options Infect Dis. 2023;15(2):27-52. DOI: 10.1007/s40506-023-00263-w.
- Yip V.C., Sanjay S., Koh Y.T. Ophthalmic complications of dengue Fever: a systematic review. Ophthalmol Ther. 2012 Dec;1(1):2. DOI: 10.1007/s40123-012-0002-z.
- Clyde K., Kyle J.L., Harris E. Recent advances in deciphering viral and host determinants of dengue virus replication and pathogenesis. J Virol. 2006 Dec;80(23):11418-31. DOI: 10.1128/JVI.01257-06.
- Mustafa M.S., Rasotgi V., Jain S., Gupta V. Discovery of fifth serotype of dengue virus (DENV-5): A new public health dilemma in dengue control. Med J Armed Forces India. 2015 Jan;71(1):67-70. DOI: 10.1016/j.mjafi.2014.09.011.
- leggi le FAQ dell'ISS
